For Living More⚕️
🚑 Εφημερεύοντα φαρμακεία / Τηλέφωνα Α’ Ανάγκης 🚑
Βρες τις χαμηλότερες τιμές φαρμάκων 💊
Λιπώδες ήπαρ: Παθογένεση και ο ρόλος των μιτοχονδρίων και του οξειδωτικού στρες
![]() 15-4-2020
15-4-2020
![]() Άννα Μαντά
Άννα Μαντά

Παθοβιοχημεία
Σαν λιπώδες ήπαρ χαρακτιρίζεται κατάσταση με παθολογική άθροιση λιπών στο ηπατικό κύτταρο. Στο φυσιολογικό ήπαρ, η ποσότητα των λιπών ανέρχεται το πολύ σε 5% του ξηρού βάρους του ενώ στο λιπώδες ήπαρ σε 40-50% του συνολικού βάρους με σχεδόν αποκλειστική παρουσία τριάκυλογλυκερίνης. Η αύξηση του λίπους μπορεί να οφείλεται σε αυξημένη σύνθεση, σε αυξημένη πρόσλψη λιπαρών οξέων και γλυκερίνης ή σε ελλατωμένη απόδοση τριακυλογλυκερινών, στη μορφή των VLDL.
Παθογένεση του λιπώδους ήπατος
|
Οξεία κατάχρηση οινοπνεύματος |
Λιπόλυση από αδρεναλίνη |
|
Χρόνια κατάχρηση οινοπνεύματος |
Αυξημένη συνθεση λιπαρών οξέων (πολύ ΝΑDH ) |
|
Έλλειψη ινσουλίνης |
Λιπόλυση στο λιπώδη ιστό |
|
Υπερσιτισμός |
Σύνθεση λιπαρών οξέων, εναποθήκευση λιπαρων οξέων |
|
Kwashiorkor |
Ελαττωμένη σύνθεση απολιποπρωτεινών |
|
Δηλητηρίαση
|
Ελαττωμένη σύνθεση απολιποπρωτεινών |
Λιπώδες ήπαρ που οφείλεται στην αλκοόλη.
Μετά από χορήγηση μεγάλων ποσοτήτων (πάνω από 120γρ) αλκοόλης, ακόμη και για μικρό χρονικό διάστημα, παρατηρείται μια φανερή αντιστρεπτή συσσώρευση λίπους στα ηπατικά κύτταρα. Αυτή οφείλεται σε αυξημένη λιπόλυση στο λιπώδη ιστο, που προκαλείται είτε από διέγερση του συμπαθητικού είτε από έκκριση αδρεναλίνης, με επακόλουθο την αυξημένη προσφορά λιπαρών οξέων και γλυκερίνης στο ήπαρ. Στο χρόνιο αλκοολισμό οι βιοχημικές διεργασίες που οδηγούν σε λιπώδες ήπαρ είναι πολυπλοκότερες. Η αποικοδόμηση της αλκοόλης με την αλκοολική αφυδρογονάση, που βρίσκεται μόνο στο ήπαρ, οδηγεί σε αυξημένο σχηματισμό ακετυλο-CoA και NADH. Με αυτό τον τρόπο διατίθεται σε αυξημένες ποσότητες το αρχικό προιόν για τη σύνθεση των λιπαρών οξέων‧επιπλέον η αύξηση του λόγου NADH/NAD⁺ ευνοεί το σχηματισμό της 3-φωσφορικής γλυκερίνης από τη φωσφορική διύδροξυακετόνη και προκαλεί αναστολή της οξειδώσεως των λιπαρών οξέων. Και οι δύο διεργασίες οδηγούν σε αυξημένη σύνθεση και εστεροποίηση των λιπαρών οξέων στο ήπαρ.
Επειδή στο χρόνιο αλκοολισμό τα λιπαρά οξέα των λιπών του ήπατος αντιστοιχούν, όσον αφορά το μήκος της αλυσίδας και το βαθμό κορεσμού, στα λιπαρά οξέα της τροφής, φαίνεται ότι και η αυξημένη απορρόφηση στο έντερο παίζει σχετικό ρόλο.
Η απόδοση των VLDL από το ήπαρ έχει περιορισθεί στο χρόνιο αλκοολισμό.
Λιπώδες ήπαρ στο διαβήτη
Στο ΣΔ αναπτύσσεται συχνά λιπώδες ήπαρ ακόμη και στο στάδιο χωρίς κλινικά συμπτώματα. Αυτό οφείλεται στην αυξημένη λιπόλυση στο λιπώδη ιστό, που έχει σαν αποτέλεσμα την αυξημένη προσφορά λιπαρών οξέων και γλυκερίνης στο ήπαρ.
Λιπώδες ήπαρ σε υπερσιτισμό
Σε υπερσιτισμό οι υδατάνθρακες και τα αμινοξέα μεταβάλλονται στο ήπαρ σε λιπαρά οξέα (λιπογένεση). Τροφή πλούσια σε λίπη οδηγεί σε υπερβολική προσφορά λιπαρών οξέων και γλυκερίνης στο ήπαρ. Σε περίπτωση δυσαρμονίας μεταξύ συνθέσεως ουδέτερων λιπών και αποδόσως VLDL, αθροίζονται λίπη στα ηπατικά κύτταρα.
Λιπώδες ήπαρ σε υποσιτισμό
Επίσης ο χρόνιος υποσιτισμός, κυρίως σε περίπτωση δίαιτας εξαιρετικά φτωχής σε πρωτείνες και πλουσιότερης σε υδατάνθρακες (Kwashiorkor) οδηγεί σε λιπώδες ήπαρ. Η ελαττωμένη σύνθεση του πρωτεινικού μέρους των λιποπρωτεινών είναι πιθανώς η αιτία για την ελαττωμένη απόδοση των τριακυλογλυκερινών από τα ηπατικά κύτταρα.
Λιπώδες ήπαρ σε δηλητηριάσεις
Σε δηλητηριάσεις με τετρακυκλίνες και αναστολείς πρωτεινοσύνθεσης (πουρομυκίνη, αιθιονίνη) δημιουργείται λιπώδες ήπαρ λόγω αναστολής της συνθέσεως των λιποπρωτεινών. Το οροτικό οξύ αναστέλλει την ενσωμάτωση γλυκοζαμίνης στις λιποπρωτεινες με αποτέλεσμα την παρεμπόδιση της λειτουργίας τους στη μεταφορά των λιπών. Μετά από την επίδραση τετραχλωράνθρακα δημιουργούνται μέσω ROS (ελευθέρων ριζών οξυγόνου) υπεροξείδια λιπιδίων στις βιομεμβράνες, κυρίως στο ενδοπλασματικό δίκτυο. Με τον τρόπο αυτό παρεμποδίζεται η σύνθεση και η απόδοση των VLDL.
Το προκαλούμενο σε πειραματόζωα, λόγω μη χορήγησης χολίνης, λιπώδες ήπαρ, οφείλεται σε έλλειψη φωσφολιπιδίων (που περιέχουν χολίνη) στις λιποπρωτείνες και στις μεμβράνες. Έτσι διαταράσσεται η μεταφορά των τριακυλογλυκερινών με τις VLDL.
Κλινική εικόνα
Λόγω της αυξημένης εναπόθεσης ουδέτερων λιπών, το ήπαρ δογκώνεται και γίνεται πιο συμπαγές. Οι λειτουργίες του ήπατος, ακόμη και σε πολύ μεγάλη λιπώση εκφύλιση, συνήθως δεν επηρεάζονται. Μόνο η δοκιμασία αποικοδόμησης της βρωμοσουλφογθαλεινης είναι συνήθως παθολογική. Η ιστολογική έρευνα για τη διαβεβαίωση της διάγνωσης δείχνει στα ηπατικά κύτταρα σταγόνες λίπους, που συμπιέζουν το κυτταρόπλασμα και τον πυρήνα προς τη περιφέρεια του κυττάρου.
Η θεραπεία του λιπώδους ήπατος συνίσταται στην αποφυγή των βλαβερών αιτιών ή σε θεραπεία της κύριας νόσου. Σε αυτές τις περιπτώσεις η συσώρρευση των τριακυλογλυκερινών είναι αντιστρεπτή.
Ο ρόλος του οξειδωτικού στρες στη παθογένεση του μη αλκοολογενούς λιπώδους ήπατος NAFLD
Η NAFLD καλύπτει ένα ευρύ φάσμα παθολογικών καταστάσεων του ήπατος που περιλαμβάνει την απλή στεάτωση (NAFL) και την στεατοηπατίτιδα (NASH), την ίνωση και τη κίρρωση. Η NAFLD έχει συνδεθεί στενά με αυξημένο κίνδυνο εμφάνισης τελικού σταδίου ηπατικής νόσου και ηπατοκυτταρικού καρκινώματος (HCG) καθώς επίσης εξωηπατικών επιπλοκών όπως καρδιαγγειακές νόσοι.
Ασθενείς με σημαντική ίνωση ή στεάτωση έχουν συγκριτικά με ασθενείς που πάσχουν από NAFL χειρότερη πρόγνωση.
Μέχρι σήμερα για τη διάγνωση της NAFLD και το διαχωρισμό της NAFL από NASH χρησιμοποιείται η βιοψία ήπατος. Συγκεκριμένα η NAFL διακρίνεται σε ποσοστό μεγαλύτερο του 5% με χαρακτηριστική μακροαγγειακή στεάτωση, ενώ η NASH σε ποσοστο μεγαλύτερο του 5% παρουσιάζεται ως ηπατική στεάτωση, φλεγμονή με ή χωρίς ίνωση. Επειδή η βιοψία είναι περιορισμένη λόγω κόστους, σφαλμάτων στα δείγματα και παρεμβατική, επιλέγονται μη παρεμβατικές μέθοδοι όπως βιοχημικές και απεικονιστικές εξετάσεις.
Με την αύξηση των ασθενών που πάσχουν από παχυσαρκία, ΣΔΤ2 και μεταβολικό σύνδρομο η NAFLD αποτελεί τη πιο συχνή χρόνια ηπατική νόσο με το ποσοστό της να ανέρχεται σε 25% παγκοσμίως
Διαταραχές στο μεταβολισμό των λιπιδίων
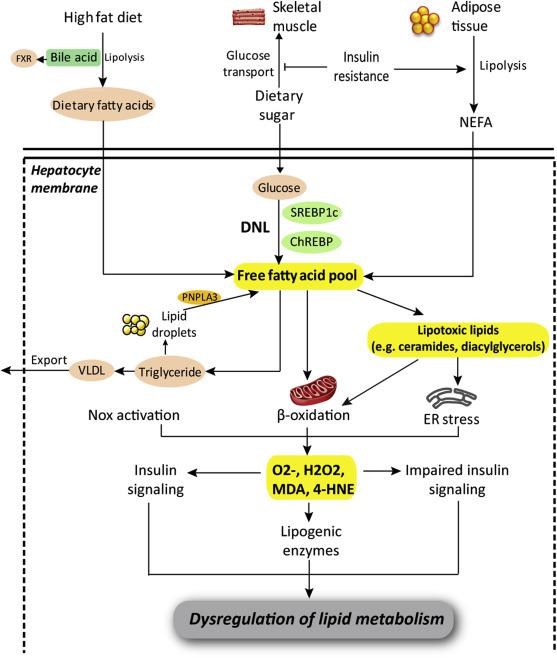
Είναι η πιο συχνή αιτία της NAFLD. Η ηπατική στεάτωση ξεκινά με έλλειψη ισορροπίας μεταξύ παραγωγής και μεταβολισμού του λίπους εξαιτίας υπερβολικής μεταβολικής δραστηριότητας του ήπατος. Για το λόγο αυτό θα πρέπει να διασαφινιστεί η προέλευση των υποστρομάτων που μεταβολίζονται στα ηπατικά κύτταρα και ειδικά τα FFAs (ελεύθερα λιπαρά οξέα). Περισσότερα από τα μισά από τα FFAs που συσωρρεύονται στο παρέγχυμα του ήπατος προέρχονται από περιφερική λιπόλυση ή NEFA.
Στη λιπόλυση των τριγλυκεριδίων παρεμβαίνει η ινσουλίνη στο λιπώδη ιστό. Συνεπώς μειωμένη ευαισθησία στην ινσουλίνη και απουσία γλυκόζης στους ιστούς χαρακτηρίζουν την αντοχή στην ινσουλίνη. Η τελευταία προκαλεί λιπόλυση χωρίς αναστολή στα κύτταρα του λιπώδους ιστού οδηγώντας σε αυξημένη μεταφορά NEFAs στο ήπαρ. Η δεύτερη μεγαλύτερη πηγή ηπατικών FFAs είναι η de novo λιπογένεση (DNL). Μέσω DNL τα ηπατοκύτταρα μετατρέπουν τη γλυκόζη και τη φρουκτόζη σε λιπαρά οξέα. Η αντοχή στην ινσουλίνη στους σκελετικούς μυς οδηγεί σε υπεργλυκαιμία και υπερινσουλιναιμία που προκαλούν την ενεργοποίηση της chEBP και sREBP1c στα ηπατοκύτταρα μέσω αύξησης της έκφρασης των λιπογονικών ενζύμων και την παραγωγή FFAs από τη γλυκόζη. Η τελευταία πηγή των FFAs είναι το διατροφικό λίπος.
Η παρουσία των FFAs αποτελεί δείκτη της ομοιόστασής τους, καθώς όταν αυτή διαταραχθεί μεγάλες ποσότητες των FFA χρησιμοποιούνται ως υποστρώματα για την παραγωγή λιποτοξικών ουσιών που προκαλούν μεταβολικό στρές, φλεγμονή και κυτταρικό θάνατο.
Οι δύο πορείες των FFAs στο ήπαρ είναι η β οξείδωση και η εστεροποίηση για τη παραγωγή τριγλυκεριδίων. Τα τριγλυκερίδια είναι τα κυριότερα συστατικά των λιποσταγονιδίων στο λιπώδες ήπαρ και ο σχηματισμός τους είναι μηχανισμός προστασίας των ηπατοκυττάρων από λιποτοξικότητα. Άλλη σημαντική προσαρμογή του λιπώδους ήπατος μπορεί να είναι η αυξημένη έξοδος τριγλυκεριδίων στη περιφέρεια με τη μορφή VLDL οδηγώντας σε υπερτριγλυκεριδαιμία.
Αλλαγές στη λειτουργία των μιτοχονδρίων
Τα μιτοχόνδρια είναι η κύρια πηγή ROS και οργανίδια υπεύθυνα για το μεταβολισμό των λιπιδίων ενώ βλάβες σε αυτά συνδέονται με τη παθογένεση στη NAFLD.
Στην απλή στεάτωση η προσαρμογή της δραστηριότητας των μιτιχονδρίων περιλαμβάνει τα εξής:
FFAs στο κυτταρόπλασμα μετατρέπονται σε λιπιδικό ακετυλο-CoA που μεταφέρεται με το σύστημα καρνιτίνης στα μιτοχόνδρια και με β-οξείδωση παράγεται ακετυλο-CoA. Περίσσεια FFA οδηγεί σε ανεπαρκή και μη αποτελεσματική β-οξείδωση με συνέπεια την παραγωγή λιποτοξικών ενδιάμεσων προιόντων. Ταυτόχρονα η πλήρης οξείδωση του ακέτυλο-CoA συνεχίζει μέσω του μιτοχονδριακού τρικαρβοξυλικού οξέος (TCA). H μιτοχονδριακή β-οξείδωση παράγει NADH και FADH2 που μεταφέρουν ηλεκτρόνια e στην αλυσίδα μεταφοράς ηλεκτρονίων ETC. Σε στενά συνδεδεμένα μιτοχόνδρια ο ρυθμός ροής των e μεσω ETC περιορίζεται από το ρυθμό επαναπρόσληψης ATP. Βλαβη στη μεταφορά e στην ETC οδηγεί σε παραγωγή ROS. Επιπλέον ένζυμα καθώς και μακράς αλυσίδας ακετυλο-CoA δεϋδρογενάση, γλυκερόλη-3φωσφατάση δεϋδρογενάση, α-κετογλουταρική δεϋδρογενάση και πυροσταφυλική δεϋδρογενάση αποτελούν πηγές ROS.

έλος στα ηπατικά μιτοχόνδρια έχουμε διαφοροποιήσεις στη δραστηριότητα της ETC, τη μιτοχονδριακή αναπνοή και την οξειδωτική φωσφορυλίωση. Για παράδιεγμα η δραστηριότητα του κυττοχρώματος c στην απλή στεάτωση μπορεί να παραμένει φυσιολογική, να αυξηθεί ή να ανασταλεί. Η κατανάλωση Ο2 από μεμονωμένα ηπατικά μιτοχόνδρια με ADP και διαφορετικά υποστρώματα αυξήθηκε, παρέμεινε σταθερή ή μειώθηκε σημαντικά. Ανάλογα συνέβει και με τη ποσότητα ATP στο ήπαρ. Οι αλλαγές αυτές βέβαια ποικίλλουν ανάλογα με τη σοβαρότητα της νόσου και το οξειδωτικό στρες.
Μεταβολές των μιτοχονδρίων στη NASH
Παρατηρούνται αλλαγές στη μιτοχονδριακή αναπνοή με εμφανή μείωση κατανάλωσης Ο2 και της δραστηριότητας της ETC. Ταυτόχρονα παρουσιάζεται έκπτωση της λειτουργίας του complex I και σταδιακά των II,III.
H ελάττωση του ATP στη NASH οφείλεται σε έκπτωση της δραστηριότγητας των συμπλεγμάτων ενώ στα αρχικά στάδια της NAFLD αυτή οφείλεται στην εγκατάλειψη της οδού της οξειδωτικής φωσφορυλίωσης λόγω επαναπρόσληψης της πρωτεϊνης UPC2 που σημμετέχει στη μεταφορά e.
Παραγωγή ROS από την ETC
Η παραγωγή των ROS εξαρτάται από το υπόστρωμα της ETC. Μια από τις συνθήκες στις οποίες έχουμε παραγωγή ROS σχετίζεται με έλλειψη μεταφορέων e όπως φλαβονοειδή (FMN), Fe–S συμπλέγματα και θέσεις Q για πρόσδεση e στα συμπλέγματα II,III.
Στόχος για τη θεραπεία της NAFLD είναι το οξειδωτικό στρες
Η αλλαγή του τρόπου ζωής με απώλεια βάρους 3-5% συνίσταται για τη βελτίωση της στεάτωσης ενώ απώλεια 7-10% απαιτείται για τη βελτίωση άλλων ιστολογικών χαρακτηριστικών της NASH, συμπεριλαμβανομένης της ίνωσης. Ο συνδυασμός διατροφής χαμηλής σε θερμιδικό φορτίο και μέτριας άσκησης φαίνεται να αποτελούν τη καλύτερη στρατηγική για τη διατήρηση της απώλειας βάρους. Η Μεσσογειακή διατροφή που χαρακτηρίζεται από περιορισμένη πρόσληψη υδατανθράκων, ειδικά απλών σακχάρων και αυξημένη κατανάλωση μονοακόρεστων και ω3 λιπαρών οξέων έχει αποδειχθεί ότι προστατεύει από τη στεάτωση ακόμη και χωρίς απώλεια βάρους, ενώ συνίσταται σε ασθενείς με NAFLD.
Επιπλέον η απώλεια βάρους με περιορισμό της θερμιδικής πρόσληψης βελτιώνει την ευασθησία στη γλυκόζη, έχει αντιοξειδωτική λειτουργία
Μία άλλη στρατηγική που έχει στόχο την απώλεια βάρους είναι η διαλλειματική νηστεία ή αλλιώς Intermittent Fasting IF. O μακροπρόθεσμος θερμικός περιορισμός συνδέεται κυρίως με την πρόληψη οξειδωτικής βλάβης ,η μακροχρόνια διαλείπουσα νηστεία προάγει την απελευθέρωση του ιστικού ROS και την τροποποίηση της οξειδωτικής πρωτεΐνης στον λιπώδη ιστό και στον σκελετικό μύ.
Συμπερασματικά
Η NAFLD αποτελεί τη πιο συχνή χρόνια ηπατική νόσο και η πρόγνωσή της συνδέέται στενά με αυξημένο κίνδυνο κίρρωσης, ηπατικού καρκινώματος και σοβαρές εξωηπατικές νόσους. Οι διαφοροποιήσεις στο οξειδωτικό στρες και τουε αντιοξειδωτικούς βιοδείκτες σε κλινικά και μοντέλα ζώων με NAFLD αποδεικνύουν στενή συσχέτιση της νόσου με τα επίπεδα οξειδωτικού στρες. Τα μιτοχόνδρια αποτελούν κύρια πηγή παραγωγής ROS και συνεπώς η δυσλειτουργία τους (αλλαγές στη μιτοχονδριακή αναπνοή,οξείδωση λιπαρών οξέων) μπορεί επικουρικά να προκαλέσει NAFLD. Παράλληλα αν και η πιο γνωστή πηγή ROS είναι η ETC του κυττάρου δεν κατηγορείται ως κύρια πηγή ROS στις ηπατικές νόσους, σε αντίθεση με τη β-οξειδωση. Το ενδοπλασματικό δίκτυο και τα NOX παρουσιάζουν λειτουργική διαφοροποίηση στη NAFLD, και αμφότερα μπορουν να παράγουν ROS, αν και η συμβολή τους στη NAFLD δεν έχει πλήρως διασαφηνιστεί. Οι συνέπειες της αυξημένης παραγωγής των ROS στη NAFLD περιλαμβάνουν τον επαναπρογρμματισμό του ηπατικού μρταβολισμού των λιπιδίων, αλλαγές στην ευαισθησία στην ινσουλίνη και φλεγμονή μέσω ενεργοποίησης με τη φυσική ανοσία.
Εφόσον ο ρόλος του οξειδωτικού στρες είναι ιδαίτερα σημαντικός στη παθογένεση της NAFLD, η χρήση αντιοξειδωτικών φαρμάκων έχει τραβήξει το ενδιαφέρον. Δυστυχώς φαρμακευτικές προσεγγίσεις που στοχεύουν εκλεκτικά οξειδωτικά μονοπάτια δεν έχουν πλήρως σχηματιστεί, ενώ υπάρχουν ακόμη κενά στη κατανόηση της παθογένεσης της NAFLD δεδομένης της πολύπλοκότητας της νόσου. Άλλωστε τα ROS περιλαμβάνουν σημαντικό αριθμό μορίων από τα οποία προκύπτουν, παράγονται σε διαφορετικά ενδοκυτταρικά συστήματα και σε διαφορετικά χρονικά διαστήματα εξέλιξης της νόσου γεγονότα που δεν επιτρέπουν τη πλήρη διασαφήνιση των δεδομένων. Για να ξεπεραστούν τα παραπάνω εμπόδια θα πρέπει να συνδιαστούν γνώσεις από τη μεταγραφομική, πρωτεομική, λιπιδομική και μεταβολομική ώστε να κατανοηθεί ο μηχανιστικός ρόλος του οξειδωτικού στρες στη NAFLD, να προσδιοριστούν θεραπευτικοί στόχοι και να κατασκευαστούν διαγνωστικοί βιοδείκτες.
Πηγές :
-
κλινική παθολογική βιοχημεία
Peter Karlson, Wolfgang Gerok, Werner Gross
-
Role of oxidative stress in the pathogenesis of nonalcoholic fatty liver disease
ZeChenac1RuifengTian ZhigangShe JingjingCaiabcHongliangLi
Κοινοποιήστε
ΔΗΜΟΦΙΛΗ ΕΒΔΟΜΑΔΑΣ
ΡΟΗ ΕΙΔΗΣΕΩΝ
| Επικοινωνία | Η ομάδα μας | Διαφημιστείτε στη truemed.gr| | Όροι χρήσης | Προσωπικά δεδομένα | Copyright©Truemed | |Για περισσότερη ζωή | Υγειά-διατροφή |
Designed – Developed by Premiumweb.gr
ΒΡΕΙΤΕ ΜΑΣ ![]()

© 2019 TrueMed Media. All rights reserved. Our website services, content, and products are for informational purposes only. TrueMed Media does not provide medical advice, diagnosis, or treatment.
Λιπώδες ήπαρ: Παθογένεση και ο ρόλος των μιτοχονδρίων και του οξειδωτικού στρες
![]() 15-4-2020
15-4-2020
![]() Άννα Μαντά
Άννα Μαντά

Παθοβιοχημεία
Σαν λιπώδες ήπαρ χαρακτιρίζεται κατάσταση με παθολογική άθροιση λιπών στο ηπατικό κύτταρο. Στο φυσιολογικό ήπαρ, η ποσότητα των λιπών ανέρχεται το πολύ σε 5% του ξηρού βάρους του ενώ στο λιπώδες ήπαρ σε 40-50% του συνολικού βάρους με σχεδόν αποκλειστική παρουσία τριάκυλογλυκερίνης. Η αύξηση του λίπους μπορεί να οφείλεται σε αυξημένη σύνθεση, σε αυξημένη πρόσλψη λιπαρών οξέων και γλυκερίνης ή σε ελλατωμένη απόδοση τριακυλογλυκερινών, στη μορφή των VLDL.
Παθογένεση του λιπώδους ήπατος
|
Οξεία κατάχρηση οινοπνεύματος |
Λιπόλυση από αδρεναλίνη |
|
Χρόνια κατάχρηση οινοπνεύματος |
Αυξημένη συνθεση λιπαρών οξέων (πολύ ΝΑDH ) |
|
Έλλειψη ινσουλίνης |
Λιπόλυση στο λιπώδη ιστό |
|
Υπερσιτισμός |
Σύνθεση λιπαρών οξέων, εναποθήκευση λιπαρων οξέων |
|
Kwashiorkor |
Ελαττωμένη σύνθεση απολιποπρωτεινών |
|
Δηλητηρίαση
|
Ελαττωμένη σύνθεση απολιποπρωτεινών |
Λιπώδες ήπαρ που οφείλεται στην αλκοόλη.
Μετά από χορήγηση μεγάλων ποσοτήτων (πάνω από 120γρ) αλκοόλης, ακόμη και για μικρό χρονικό διάστημα, παρατηρείται μια φανερή αντιστρεπτή συσσώρευση λίπους στα ηπατικά κύτταρα. Αυτή οφείλεται σε αυξημένη λιπόλυση στο λιπώδη ιστο, που προκαλείται είτε από διέγερση του συμπαθητικού είτε από έκκριση αδρεναλίνης, με επακόλουθο την αυξημένη προσφορά λιπαρών οξέων και γλυκερίνης στο ήπαρ. Στο χρόνιο αλκοολισμό οι βιοχημικές διεργασίες που οδηγούν σε λιπώδες ήπαρ είναι πολυπλοκότερες. Η αποικοδόμηση της αλκοόλης με την αλκοολική αφυδρογονάση, που βρίσκεται μόνο στο ήπαρ, οδηγεί σε αυξημένο σχηματισμό ακετυλο-CoA και NADH. Με αυτό τον τρόπο διατίθεται σε αυξημένες ποσότητες το αρχικό προιόν για τη σύνθεση των λιπαρών οξέων‧επιπλέον η αύξηση του λόγου NADH/NAD⁺ ευνοεί το σχηματισμό της 3-φωσφορικής γλυκερίνης από τη φωσφορική διύδροξυακετόνη και προκαλεί αναστολή της οξειδώσεως των λιπαρών οξέων. Και οι δύο διεργασίες οδηγούν σε αυξημένη σύνθεση και εστεροποίηση των λιπαρών οξέων στο ήπαρ.
Επειδή στο χρόνιο αλκοολισμό τα λιπαρά οξέα των λιπών του ήπατος αντιστοιχούν, όσον αφορά το μήκος της αλυσίδας και το βαθμό κορεσμού, στα λιπαρά οξέα της τροφής, φαίνεται ότι και η αυξημένη απορρόφηση στο έντερο παίζει σχετικό ρόλο.
Η απόδοση των VLDL από το ήπαρ έχει περιορισθεί στο χρόνιο αλκοολισμό.
Λιπώδες ήπαρ στο διαβήτη
Στο ΣΔ αναπτύσσεται συχνά λιπώδες ήπαρ ακόμη και στο στάδιο χωρίς κλινικά συμπτώματα. Αυτό οφείλεται στην αυξημένη λιπόλυση στο λιπώδη ιστό, που έχει σαν αποτέλεσμα την αυξημένη προσφορά λιπαρών οξέων και γλυκερίνης στο ήπαρ.
Λιπώδες ήπαρ σε υπερσιτισμό
Σε υπερσιτισμό οι υδατάνθρακες και τα αμινοξέα μεταβάλλονται στο ήπαρ σε λιπαρά οξέα (λιπογένεση). Τροφή πλούσια σε λίπη οδηγεί σε υπερβολική προσφορά λιπαρών οξέων και γλυκερίνης στο ήπαρ. Σε περίπτωση δυσαρμονίας μεταξύ συνθέσεως ουδέτερων λιπών και αποδόσως VLDL, αθροίζονται λίπη στα ηπατικά κύτταρα.
Λιπώδες ήπαρ σε υποσιτισμό
Επίσης ο χρόνιος υποσιτισμός, κυρίως σε περίπτωση δίαιτας εξαιρετικά φτωχής σε πρωτείνες και πλουσιότερης σε υδατάνθρακες (Kwashiorkor) οδηγεί σε λιπώδες ήπαρ. Η ελαττωμένη σύνθεση του πρωτεινικού μέρους των λιποπρωτεινών είναι πιθανώς η αιτία για την ελαττωμένη απόδοση των τριακυλογλυκερινών από τα ηπατικά κύτταρα.
Λιπώδες ήπαρ σε δηλητηριάσεις
Σε δηλητηριάσεις με τετρακυκλίνες και αναστολείς πρωτεινοσύνθεσης (πουρομυκίνη, αιθιονίνη) δημιουργείται λιπώδες ήπαρ λόγω αναστολής της συνθέσεως των λιποπρωτεινών. Το οροτικό οξύ αναστέλλει την ενσωμάτωση γλυκοζαμίνης στις λιποπρωτεινες με αποτέλεσμα την παρεμπόδιση της λειτουργίας τους στη μεταφορά των λιπών. Μετά από την επίδραση τετραχλωράνθρακα δημιουργούνται μέσω ROS (ελευθέρων ριζών οξυγόνου) υπεροξείδια λιπιδίων στις βιομεμβράνες, κυρίως στο ενδοπλασματικό δίκτυο. Με τον τρόπο αυτό παρεμποδίζεται η σύνθεση και η απόδοση των VLDL.
Το προκαλούμενο σε πειραματόζωα, λόγω μη χορήγησης χολίνης, λιπώδες ήπαρ, οφείλεται σε έλλειψη φωσφολιπιδίων (που περιέχουν χολίνη) στις λιποπρωτείνες και στις μεμβράνες. Έτσι διαταράσσεται η μεταφορά των τριακυλογλυκερινών με τις VLDL.
Κλινική εικόνα
Λόγω της αυξημένης εναπόθεσης ουδέτερων λιπών, το ήπαρ δογκώνεται και γίνεται πιο συμπαγές. Οι λειτουργίες του ήπατος, ακόμη και σε πολύ μεγάλη λιπώση εκφύλιση, συνήθως δεν επηρεάζονται. Μόνο η δοκιμασία αποικοδόμησης της βρωμοσουλφογθαλεινης είναι συνήθως παθολογική. Η ιστολογική έρευνα για τη διαβεβαίωση της διάγνωσης δείχνει στα ηπατικά κύτταρα σταγόνες λίπους, που συμπιέζουν το κυτταρόπλασμα και τον πυρήνα προς τη περιφέρεια του κυττάρου.
Η θεραπεία του λιπώδους ήπατος συνίσταται στην αποφυγή των βλαβερών αιτιών ή σε θεραπεία της κύριας νόσου. Σε αυτές τις περιπτώσεις η συσώρρευση των τριακυλογλυκερινών είναι αντιστρεπτή.
Ο ρόλος του οξειδωτικού στρες στη παθογένεση του μη αλκοολογενούς λιπώδους ήπατος NAFLD
Η NAFLD καλύπτει ένα ευρύ φάσμα παθολογικών καταστάσεων του ήπατος που περιλαμβάνει την απλή στεάτωση (NAFL) και την στεατοηπατίτιδα (NASH), την ίνωση και τη κίρρωση. Η NAFLD έχει συνδεθεί στενά με αυξημένο κίνδυνο εμφάνισης τελικού σταδίου ηπατικής νόσου και ηπατοκυτταρικού καρκινώματος (HCG) καθώς επίσης εξωηπατικών επιπλοκών όπως καρδιαγγειακές νόσοι.
Ασθενείς με σημαντική ίνωση ή στεάτωση έχουν συγκριτικά με ασθενείς που πάσχουν από NAFL χειρότερη πρόγνωση.
Μέχρι σήμερα για τη διάγνωση της NAFLD και το διαχωρισμό της NAFL από NASH χρησιμοποιείται η βιοψία ήπατος. Συγκεκριμένα η NAFL διακρίνεται σε ποσοστό μεγαλύτερο του 5% με χαρακτηριστική μακροαγγειακή στεάτωση, ενώ η NASH σε ποσοστο μεγαλύτερο του 5% παρουσιάζεται ως ηπατική στεάτωση, φλεγμονή με ή χωρίς ίνωση. Επειδή η βιοψία είναι περιορισμένη λόγω κόστους, σφαλμάτων στα δείγματα και παρεμβατική, επιλέγονται μη παρεμβατικές μέθοδοι όπως βιοχημικές και απεικονιστικές εξετάσεις.
Με την αύξηση των ασθενών που πάσχουν από παχυσαρκία, ΣΔΤ2 και μεταβολικό σύνδρομο η NAFLD αποτελεί τη πιο συχνή χρόνια ηπατική νόσο με το ποσοστό της να ανέρχεται σε 25% παγκοσμίως
Διαταραχές στο μεταβολισμό των λιπιδίων
Είναι η πιο συχνή αιτία της NAFLD. Η ηπατική στεάτωση ξεκινά με έλλειψη ισορροπίας μεταξύ παραγωγής και μεταβολισμού του λίπους εξαιτίας υπερβολικής μεταβολικής δραστηριότητας του ήπατος. Για το λόγο αυτό θα πρέπει να διασαφινιστεί η προέλευση των υποστρομάτων που μεταβολίζονται στα ηπατικά κύτταρα και ειδικά τα FFAs (ελεύθερα λιπαρά οξέα). Περισσότερα από τα μισά από τα FFAs που συσωρρεύονται στο παρέγχυμα του ήπατος προέρχονται από περιφερική λιπόλυση ή NEFA.
Στη λιπόλυση των τριγλυκεριδίων παρεμβαίνει η ινσουλίνη στο λιπώδη ιστό. Συνεπώς μειωμένη ευαισθησία στην ινσουλίνη και απουσία γλυκόζης στους ιστούς χαρακτηρίζουν την αντοχή στην ινσουλίνη. Η τελευταία προκαλεί λιπόλυση χωρίς αναστολή στα κύτταρα του λιπώδους ιστού οδηγώντας σε αυξημένη μεταφορά NEFAs στο ήπαρ. Η δεύτερη μεγαλύτερη πηγή ηπατικών FFAs είναι η de novo λιπογένεση (DNL). Μέσω DNL τα ηπατοκύτταρα μετατρέπουν τη γλυκόζη και τη φρουκτόζη σε λιπαρά οξέα. Η αντοχή στην ινσουλίνη στους σκελετικούς μυς οδηγεί σε υπεργλυκαιμία και υπερινσουλιναιμία που προκαλούν την ενεργοποίηση της chEBP και sREBP1c στα ηπατοκύτταρα μέσω αύξησης της έκφρασης των λιπογονικών ενζύμων και την παραγωγή FFAs από τη γλυκόζη. Η τελευταία πηγή των FFAs είναι το διατροφικό λίπος.
Η παρουσία των FFAs αποτελεί δείκτη της ομοιόστασής τους, καθώς όταν αυτή διαταραχθεί μεγάλες ποσότητες των FFA χρησιμοποιούνται ως υποστρώματα για την παραγωγή λιποτοξικών ουσιών που προκαλούν μεταβολικό στρές, φλεγμονή και κυτταρικό θάνατο.
Οι δύο πορείες των FFAs στο ήπαρ είναι η β οξείδωση και η εστεροποίηση για τη παραγωγή τριγλυκεριδίων. Τα τριγλυκερίδια είναι τα κυριότερα συστατικά των λιποσταγονιδίων στο λιπώδες ήπαρ και ο σχηματισμός τους είναι μηχανισμός προστασίας των ηπατοκυττάρων από λιποτοξικότητα. Άλλη σημαντική προσαρμογή του λιπώδους ήπατος μπορεί να είναι η αυξημένη έξοδος τριγλυκεριδίων στη περιφέρεια με τη μορφή VLDL οδηγώντας σε υπερτριγλυκεριδαιμία.

Αλλαγές στη λειτουργία των μιτοχονδρίων
Τα μιτοχόνδρια είναι η κύρια πηγή ROS και οργανίδια υπεύθυνα για το μεταβολισμό των λιπιδίων ενώ βλάβες σε αυτά συνδέονται με τη παθογένεση στη NAFLD.
Στην απλή στεάτωση η προσαρμογή της δραστηριότητας των μιτιχονδρίων περιλαμβάνει τα εξής:
FFAs στο κυτταρόπλασμα μετατρέπονται σε λιπιδικό ακετυλο-CoA που μεταφέρεται με το σύστημα καρνιτίνης στα μιτοχόνδρια και με β-οξείδωση παράγεται ακετυλο-CoA. Περίσσεια FFA οδηγεί σε ανεπαρκή και μη αποτελεσματική β-οξείδωση με συνέπεια την παραγωγή λιποτοξικών ενδιάμεσων προιόντων. Ταυτόχρονα η πλήρης οξείδωση του ακέτυλο-CoA συνεχίζει μέσω του μιτοχονδριακού τρικαρβοξυλικού οξέος (TCA). H μιτοχονδριακή β-οξείδωση παράγει NADH και FADH2 που μεταφέρουν ηλεκτρόνια e στην αλυσίδα μεταφοράς ηλεκτρονίων ETC. Σε στενά συνδεδεμένα μιτοχόνδρια ο ρυθμός ροής των e μεσω ETC περιορίζεται από το ρυθμό επαναπρόσληψης ATP. Βλαβη στη μεταφορά e στην ETC οδηγεί σε παραγωγή ROS. Επιπλέον ένζυμα καθώς και μακράς αλυσίδας ακετυλο-CoA δεϋδρογενάση, γλυκερόλη-3φωσφατάση δεϋδρογενάση, α-κετογλουταρική δεϋδρογενάση και πυροσταφυλική δεϋδρογενάση αποτελούν πηγές ROS.

έλος στα ηπατικά μιτοχόνδρια έχουμε διαφοροποιήσεις στη δραστηριότητα της ETC, τη μιτοχονδριακή αναπνοή και την οξειδωτική φωσφορυλίωση. Για παράδιεγμα η δραστηριότητα του κυττοχρώματος c στην απλή στεάτωση μπορεί να παραμένει φυσιολογική, να αυξηθεί ή να ανασταλεί. Η κατανάλωση Ο2 από μεμονωμένα ηπατικά μιτοχόνδρια με ADP και διαφορετικά υποστρώματα αυξήθηκε, παρέμεινε σταθερή ή μειώθηκε σημαντικά. Ανάλογα συνέβει και με τη ποσότητα ATP στο ήπαρ. Οι αλλαγές αυτές βέβαια ποικίλλουν ανάλογα με τη σοβαρότητα της νόσου και το οξειδωτικό στρες.
Μεταβολές των μιτοχονδρίων στη NASH
Παρατηρούνται αλλαγές στη μιτοχονδριακή αναπνοή με εμφανή μείωση κατανάλωσης Ο2 και της δραστηριότητας της ETC. Ταυτόχρονα παρουσιάζεται έκπτωση της λειτουργίας του complex I και σταδιακά των II,III.
H ελάττωση του ATP στη NASH οφείλεται σε έκπτωση της δραστηριότγητας των συμπλεγμάτων ενώ στα αρχικά στάδια της NAFLD αυτή οφείλεται στην εγκατάλειψη της οδού της οξειδωτικής φωσφορυλίωσης λόγω επαναπρόσληψης της πρωτεϊνης UPC2 που σημμετέχει στη μεταφορά e.
Παραγωγή ROS από την ETC
Η παραγωγή των ROS εξαρτάται από το υπόστρωμα της ETC. Μια από τις συνθήκες στις οποίες έχουμε παραγωγή ROS σχετίζεται με έλλειψη μεταφορέων e όπως φλαβονοειδή (FMN), Fe–S συμπλέγματα και θέσεις Q για πρόσδεση e στα συμπλέγματα II,III.
Στόχος για τη θεραπεία της NAFLD είναι το οξειδωτικό στρες
Η αλλαγή του τρόπου ζωής με απώλεια βάρους 3-5% συνίσταται για τη βελτίωση της στεάτωσης ενώ απώλεια 7-10% απαιτείται για τη βελτίωση άλλων ιστολογικών χαρακτηριστικών της NASH, συμπεριλαμβανομένης της ίνωσης. Ο συνδυασμός διατροφής χαμηλής σε θερμιδικό φορτίο και μέτριας άσκησης φαίνεται να αποτελούν τη καλύτερη στρατηγική για τη διατήρηση της απώλειας βάρους. Η Μεσσογειακή διατροφή που χαρακτηρίζεται από περιορισμένη πρόσληψη υδατανθράκων, ειδικά απλών σακχάρων και αυξημένη κατανάλωση μονοακόρεστων και ω3 λιπαρών οξέων έχει αποδειχθεί ότι προστατεύει από τη στεάτωση ακόμη και χωρίς απώλεια βάρους, ενώ συνίσταται σε ασθενείς με NAFLD.
Επιπλέον η απώλεια βάρους με περιορισμό της θερμιδικής πρόσληψης βελτιώνει την ευασθησία στη γλυκόζη, έχει αντιοξειδωτική λειτουργία
Μία άλλη στρατηγική που έχει στόχο την απώλεια βάρους είναι η διαλλειματική νηστεία ή αλλιώς Intermittent Fasting IF. O μακροπρόθεσμος θερμικός περιορισμός συνδέεται κυρίως με την πρόληψη οξειδωτικής βλάβης ,η μακροχρόνια διαλείπουσα νηστεία προάγει την απελευθέρωση του ιστικού ROS και την τροποποίηση της οξειδωτικής πρωτεΐνης στον λιπώδη ιστό και στον σκελετικό μύ.
Συμπερασματικά
Η NAFLD αποτελεί τη πιο συχνή χρόνια ηπατική νόσο και η πρόγνωσή της συνδέέται στενά με αυξημένο κίνδυνο κίρρωσης, ηπατικού καρκινώματος και σοβαρές εξωηπατικές νόσους. Οι διαφοροποιήσεις στο οξειδωτικό στρες και τουε αντιοξειδωτικούς βιοδείκτες σε κλινικά και μοντέλα ζώων με NAFLD αποδεικνύουν στενή συσχέτιση της νόσου με τα επίπεδα οξειδωτικού στρες. Τα μιτοχόνδρια αποτελούν κύρια πηγή παραγωγής ROS και συνεπώς η δυσλειτουργία τους (αλλαγές στη μιτοχονδριακή αναπνοή,οξείδωση λιπαρών οξέων) μπορεί επικουρικά να προκαλέσει NAFLD. Παράλληλα αν και η πιο γνωστή πηγή ROS είναι η ETC του κυττάρου δεν κατηγορείται ως κύρια πηγή ROS στις ηπατικές νόσους, σε αντίθεση με τη β-οξειδωση. Το ενδοπλασματικό δίκτυο και τα NOX παρουσιάζουν λειτουργική διαφοροποίηση στη NAFLD, και αμφότερα μπορουν να παράγουν ROS, αν και η συμβολή τους στη NAFLD δεν έχει πλήρως διασαφηνιστεί. Οι συνέπειες της αυξημένης παραγωγής των ROS στη NAFLD περιλαμβάνουν τον επαναπρογρμματισμό του ηπατικού μρταβολισμού των λιπιδίων, αλλαγές στην ευαισθησία στην ινσουλίνη και φλεγμονή μέσω ενεργοποίησης με τη φυσική ανοσία.
Εφόσον ο ρόλος του οξειδωτικού στρες είναι ιδαίτερα σημαντικός στη παθογένεση της NAFLD, η χρήση αντιοξειδωτικών φαρμάκων έχει τραβήξει το ενδιαφέρον. Δυστυχώς φαρμακευτικές προσεγγίσεις που στοχεύουν εκλεκτικά οξειδωτικά μονοπάτια δεν έχουν πλήρως σχηματιστεί, ενώ υπάρχουν ακόμη κενά στη κατανόηση της παθογένεσης της NAFLD δεδομένης της πολύπλοκότητας της νόσου. Άλλωστε τα ROS περιλαμβάνουν σημαντικό αριθμό μορίων από τα οποία προκύπτουν, παράγονται σε διαφορετικά ενδοκυτταρικά συστήματα και σε διαφορετικά χρονικά διαστήματα εξέλιξης της νόσου γεγονότα που δεν επιτρέπουν τη πλήρη διασαφήνιση των δεδομένων. Για να ξεπεραστούν τα παραπάνω εμπόδια θα πρέπει να συνδιαστούν γνώσεις από τη μεταγραφομική, πρωτεομική, λιπιδομική και μεταβολομική ώστε να κατανοηθεί ο μηχανιστικός ρόλος του οξειδωτικού στρες στη NAFLD, να προσδιοριστούν θεραπευτικοί στόχοι και να κατασκευαστούν διαγνωστικοί βιοδείκτες.
Πηγές :
-
κλινική παθολογική βιοχημεία
Peter Karlson, Wolfgang Gerok, Werner Gross
-
Role of oxidative stress in the pathogenesis of nonalcoholic fatty liver disease
ZeChenac1RuifengTian ZhigangShe JingjingCaiabcHongliangLi
Κοινοποιήστε
ΔΙΑΒΑΣΤΕ ΕΠΙΣΗΣ
© 2019 TrueMed Media. All rights reserved. Our website services, content, and products are for informational purposes only. TrueMed Media does not provide medical advice, diagnosis, or treatment.

Αρθρογράφος
Γεννηθείσα 16/06/1999 στο Μαρούσι Αττικής με τόπο καταγωγής τη Χαλκίδα, Ευβοίας. Από μικρή απολάμβανε την επαφή με τη φύση, τα ντοκιμαντερ και τη ζωγραφική.
Η αγάπη για την ιατρική και το ανθρώπινο σώμα ξεκίνησε από πολύ νωρίς να εμφανίζεται, επηρεασμένη από γονεϊκά πρότυπα. Στο γυμνάσιο και το λύκειο ήρθε σε επαφή με το αντικείμενο παρακολουθώντας Χειρουργικές επεμβάσεις.
Ως φοιτήτρια Ιατρικής στο ΔΠΘ σήμερα προσπαθεί να κατανοήσει σε βάθος τη πολυπλοκότητα αυτής Επιστήμης αυτής, έχοντας θάρρος, όρεξη και αγάπη γι’ αυτή.
Βασική εκπαίδευση
2007-2013:7ΟΔΗΜΟΤΙΚΟ ΧΑΛΚΙΔΑΣ
2013-2015:1ΟΓΥΜΑΝΣΙΟ ΧΑΛΚΙΔΑΣ
2015-2017: 1οΓΕΛ ΧΑΛΚΙΔΑΣ
ΠΑΝΕΠΙΣΤΗΜΙΑΚΕΣ ΣΠΟΥΔΕΣ
ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΔΗΜΟΚΡΙΤΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΡΑΚΗΣ
ΕΤΟΣ ΕΙΣΑΓΩΓΗΣ: 2017
ΞΈΝΕΣ ΓΛΩΣΣΕΣ
Αγγλικά : FCE (Cambridge English: First), επιπέδου B2 (University of Cambridge)
Γερμανικά: Goethe-Zertifikat B2
Συμμετοχή και Παρακολούθηση
- Ομιλία «Η Ανοσοθεραπεία στο Καρκίνο της Ουροδόχου Κύστεως και Νεφρών» στο 10o ΣΥΝΕΔΡΙΟ Ε.Δ.Ε.Μ.Σ.Ε.Θ., 7-8 Μαΐου 2021
- Συμμετοχή και Παρακολούθηση στο 27ο Επιστημονικό Συνέδριο Φοιτητών Ιατρικής Ελλάδας & 15ο Διεθνές Forum Φοιτητών Ιατρικής και Νέων Ιατρών
Ομιλία «Πρόληψη Σεξουαλικής Κακοποίησης Ανηλίκων» Τράπεζα Ιατροδικαστικής
- Συμμετοχή στο Webinar Παχυσαρκία: Από την Αιτιοπαθογένεια στη Θεραπεία 24/04/ 2021
- Συμμετοχή στην Ημερίδα Απεικόνιση Παιδιατρικού Θώρακα: Από την πλευρά του Παιδιάτρου και του Ακτινολόγου 3/04/ 2021
- Συμμετοχή στη διοργάνωση του Webinar της ΕΕΦΙΕ του παραρτήματος Αλεξανδρούπολης "Επείγοντα περιστατικά με Έμφαση στο αγροτικό"
- Παρακολούθηση:Η Παθολογία της Κύησης σε 40 Ερωτήσεις (WEB CONGRESS) // 5-6-7 /03/ 2021
- Συμμετοχή στο 29ο Πανελλήνιο Πνευμονολογικό Συνέδριο
- Παρακολούθηση KIDS SAVE LIVES - Τα Παιδιά Σώζουν Ζωές
- Ομιλία «ΙΦΝΕ και COVID-19» στο 1o Πανελλήνιο Διαδικτυακό Συνέδριο Ιατρικής Βιοπαθολογίας, το οποίο διοργανώθηκε από την Πανελλήνια Ένωση Ιατρικής Βιοπαθολογίας και την Ελληνική Εταιρεία Ιατρικής Βιοπαθολογίας/ Εργαστηριακής Ιατρικής διαδικτυακά στις 11-13 Δεκεμβρίου 2020.
- Παρακολούθηση στο 25ου Επιστημονικό Συνέδριο Φοιτητών Ιατρικής Ελλάδας & 15ο Διεθνές Forum Φοιτητών Ιατρικής και Νέων Ιατρών
Αριθμός άρθρων που έχει γράψει στην Truemed: 2