Το λίπος… απλά αποθήκη ενέργειας; (Ο ρόλος του στον οργανισμό)
![]() 23-11-2020
23-11-2020
![]() Άννα Μαντά
Άννα Μαντά
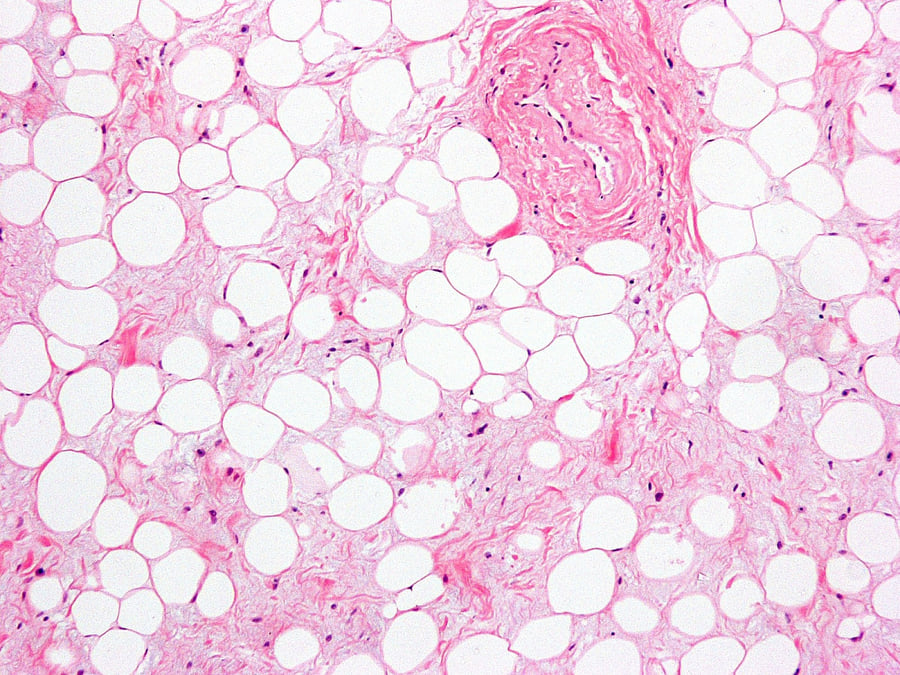
Ο λιπώδης ιστός ο οποίος κάποτε θεωρείτο αδρανές όργανο αποθήκευσης ενέργειας που παρέχει μόνωση από το κρύο, αναγνωρίζεται πλέον ως ένα δυναμικό ενδοκρινικό σύστημα.
Αποτελείται από πολλά κύτταρα συμπεριλαμβανομένων των λιποκυττάρων, των προ-λιποκυττάρων, των ενδοθηλιακών κυττάρων, των μονοκυττάρων, των μακροφάγων και του ινοβλαστικού συνδετικού ιστού.

Η λιπογένεση αναφέρεται στη διαφοροποίηση των προ-αδιποκυττάρων σε ώριμα λιποκύτταρα με σκοπό την ανάπτυξη του λιπώδους ιστού, γεγονός που διαφοροποιείται ανάλογα με το φύλο και την ηλικία. Τα λιποκύτταρα διαφοροποιούνται από αστεροειδή και ατρακτοειδή πρόδρομα κύτταρα μεσεγχυματικής προέλευσης.
Τα προ-αδιποκύτταρα στο λιπώδη ιστό μπορούν να διαφοροποιηθούν σε ώριμα αδιποκύτταρα κατά τη διάρκεια της ζωής, επιτρέποντας έτσι την υπερπλασία του λιπώδους ιστού όταν οι ανάγκες για αποθήκευση ενέργειας αυξάνονται. Επιπλέον τα ώριμα λιποκύτταρα μπορούν να αυξηθούν σε μέγεθος σε καταστάσεις όπως η υπερβολική θρέψη με αποτέλεσμα να γίνονται υπερτροφικά. Τελικά ο αριθμός των λιποκυττάρων και η μορφολογία τους ρυθμίζεται από βιοχημικές διαδικασίες όπως η εστεροποίηση, λιπόλυση και διαφοροποίηση των προ-αδιποκυττάρων, ως απάντηση σε αλλαγές της ενεργειακής ισορροπίας.
Υπάρχουν δύο τύποι ώριμων λιποκυττάρων στα θηλαστικά: τα καφέ και τα λευκά λιποκύτταρα
Τα καφέ λιποκύτταρα είναι πιο άφθονα στη παιδική ηλικία, αλλά αντιπροσωπεύονται ελάχιστα στους ενήλικες, εμπλέκονται στη βασική παραγωγή θερμότητας, ενώ τα λευκά χρησιμεύουν ως μακροπρόθεσμη δεξαμενή καυσίμων.
Γυναίκες και άνδρες παρουσιάζουν διμορφική σύνθεση του σωματικού τους λίπους, με τους άνδρες να έχουν κεντρική ή κοιλιακή παχυσαρκία, ενώ οι γυναίκες έχουν περισσότερο λίπος στη περιοχή των μηρών και των γλουτών.
Τα λευκά λιποκύτταρα παράγουν πολυάριθμα ενδοκρινικά, παρακρινικά και νευροενδοκρινικά σήματα μέσω της παραγωγής αδιποκινών.
Οι αδιποκίνες περιλαμβάνουν οποιαδήποτε ουσία που απελευθερώνεται από το λιπώδη ιστό, είτε από τα λιποκύτταρα, διηθητικά μακροφάγα, στρωματικά κύτταρα ή άλλα μέρη του λιπώδους ιστού (συνδετικός ιστός και αιμοφόρα αγγεία).
Αυτές οι ουσίες περιλαμβάνουν κυτταροκίνες, αυξητικούς παράγοντες, χημειοκίνες, παράγοντες συμπληρώματος και πρωτεΐνες που εμπλέκονται στην αγγειακή αιμόσταση, στη ρύθμιση της αρτηριακής πίεσης, το μεταβολισμό των λιπιδίων, την ομοιοστασία της γλυκόζης, στη φλεγμονή, στην αγγειογένεση και στην αναπαραγωγή
Οι ποσότητες των αδιποκινών μπορεί να ποικίλουν ανάλογα με τη μεταβολική κατάσταση (πχ. Νοσογόνος παχυσαρκία), το διαμέρισμα του λίπους (σπαλχνικό,υποδόριο) και την ανάπτυξη των κυττάρων (προλιποκύτταρα, ώριμα λιποκύτταρα).
Ορισμένες αδιποκίνες απελευθερώνονται σε σημαντικές ποσότητες στη κυκλοφορία (πχ λεπτίνη, αδιπονεκτίνη), ενώ άλλες όπως ο TNF–a, παραμένουν κυρίως εντοπισμένες στο λιπώδη ιστό και λειτουργούν ως παρακρινικοί ή αυτοκρινικοί ρυθμιστές.
Ο αριθμός των αδιποκινών εξελίσσεται (>600 πιθανοί διαμεσολαβητές σηματοδότησης κυττάρων) και αρκετές αδιποκίνες αναγνωρίζονται σήμερα ως πιθανοί μεσολαβητές της αναπαραγωγικής υγείας και των αναπαραγωγικών διαταραχών.

Η λεπτίνη είναι μία ορμόνη που αποτελείται από 167 αμινοξέα και συντίθεται στο λευκό λιπώδη ιστό, συμμετέχει στη ρύθμιση πρόσληψης τροφής και ενεργειακής ομοιόστασης ενεργώντας στο ΚΝΣ. Η λεπτίνη και το γονίδιό της (obesity gene) ανακαλύφθηκαν το 1994. Η έκφραση του γονιδίου της λεπτίνης ρυθμίζεται από μία ποικιλία ορμονών, κυτταροκινών και αυξητικών παραγόντων. Τα οιστρογόνα επάγουν, ενώ τα ανδρογόνα καταστέλλουν τη παραγωγή λεπτίνης, παρέχοντας μία εξήγηση για το σεξουαλικό διμορφισμό σε επίπεδα λεπτίνης στον ορό.

Οι μεταλλάξεις σε αυτό το γονίδιο προκαλούν νοσογόνο παχυσαρκία και διαβήτη σε ανθρώπους και ζώα. Αν και η λεπτίνη είχε αρχικά θεωρηθεί οτί εκφράζεται αποκλειστικά στο λευκό λιπώδη ιστό, μεταγενέστερες αναφορές έδειξαν ότι η λεπτίνη εκφράζεται και σε άλλες περιοχές, όπως ο υποθάλαμος, η υπόφυση, το γαστρικό επιθήλιο, οι σκελετικοί μυς, ο πλακούντας, ο μαστός και οι γονάδες.
Η λεπτίνη εκκρίνεται με παλμικό τρόπο με σημαντική ημερήσια διακύμανση (χαμηλότερα επίπεδα στα μέσα του απογεύματος και υψηλότερα επίπεδα τα μεσάνυκτα). Η στάθμη της στον ορό σχετίζεται με τη ποσότητα και τη κατανομή της μάζας του σωματικού λίπους, παρέχοντας ένα περιφερειακό σήμα στο ΚΝΣ σχετικά με την επάρκεια της διατροφικής κατάστασης. Επιπλέον η ορμόνη εμπλέκεται στον έλεγχο πολλών φυσιολογικών λειτουργιών, όπως η ανάπτυξη, ο μεταβολισμός και η αναπαραγωγή.
Υποδοχείς λεπτίνης
Οι υποδοχείς λεπτίνης (ObRs) ανήκουν στην οικογένεια υποδοχέων κυταροκίνης και εντοπίζονται στο ΚΝΣ και σε περιφερικούς ιστούς. Υπάρχουν 6 ισομορφές του υποδοχέα λεπτίνης (4 μορφές έχουν βρεθεί στον άνθρωπο), οι οποίες έχουν μια εξωκυττάρια περιοχή και είτε δεν έχουν τη διαμεμβρανική περιοχή (ObRe, ισομορφή που αντιπροσωπεύει τη κυκλοφορούσα μορφή του Ob–R)είτε έχουν διαφορετικά μήκη της ενδοκυτταρικής περιοχής (Οb–Ra,bc,d,f). H λεπτίνη κυκλοφορεί στα βιολογικά υγρά τόσο ως ελεύθερη όσο και σε μορφή που δεσμεύεται με τη διαλυτή ισομορφή του υποδοχέα της (Οb–Re).
Οι υποδοχείς της λεπτίνης εκφράζονται σε όλο το σώμα, συμπεριλαμβανομένου του ΚΝΣ, όπου η λεπτίνη δρα για τη ρύθμιση της νευροενδοκρινικής λειτουργίας, της διατροφικής συμπεριφοράς και της ενεργειακής δαπάνης. Η λεπτίνη εκτελεί τη δράση της μέσω του υποδοχέα της, ο οποίος με τη σειρά του ενεργοποιεί πολλές ενδοκυτταρικές οδούς σηματοδότησης.
Ακόμη οι υποδοχείς της λεπτίνης (ObRs) έχουν ταυτοποιηθεί στον υποθάλαμο, στα γοναδοτρόπα κύτταρα της πρόσθιας υπόφυσης, στα κοκκιώδη κύτταρα, στα κύτταρα της θήκης και στο ενδομήτριο. Αυτή η πολυεστιακή έκφραση της λεπτίνης, καθώς και η πυκνή παρουσία Ob–Rs σε όλα τα επίπεδα του άξονα υποθαλάμου-υπόφυση-γονάδες (HPG), υποδηλώνει ότι η ρύθμιση της αναπαραγωγής μέσω της λεπτίνης περιλαμβάνει ένα περίπλοκο δίκτυο αλληλεπιδράσεων σε πολλαπλά επίπεδα για να ρυθμίσει τον άξονα HPG με παρακρινικό ή/και ενδοκρινικό τρόπο.
Τα παχύσαρκα άτομα παρουσιάζουν υψηλά επίπεδα έκφρασης της λεπτίνης στο λιπώδη ιστό και έχουν αυξημένα επίπεδα λεπτίνης στη κυκλοφορία, όμως αυτά τα επίπεδα αποτυγχάνουν να μειώσουν τη περίσσεια του λίπους, εμφανίζοντας αντίσταση στη λεπτίνη. H λεπτίνη αυξάνεται από τα γλυκοκορτικοειδή, στην οξεία λοίμωξη και από προ-φλεγμονώδεις κυτταροκίνες. Αντίθετα η έκθεση στο κρύο, η αδρενεργική διέγερση, η αυξητική ορμόνη, οι ορμόνες του θυρεοειδούς, η μελατονίνη, το κάπνισμα και οι θειαζολιδινεδιόνες μειώνουν τα επίπεδα λεπτίνης. Τα επίπεδά της είναι υψηλότερα στις γυναίκες σε σύγκριση με τους άνδρες, εν μέρη λόγω της αναστολής της από τα ανδρογόνα, τη διέγερσή της από τα οιστρογόνα και λόγω των διαφορών στην έκφρασή της ανάμεσα στα δύο φύλα. Επίσης η λεπτίνη συντίθεται σε μεγαλύτερο ποσοστό στο υποδόριο λίπος παρά στο σπλαχνικό, γεγονός που εξηγεί και τα υψηλότερα επίπεδά της στις γυναίκες λόγω αυξημένου υποδόριου λίπους.
Στη περίπτωση της γυναικείας υπογονιμότητας, η λεπτίνη είναι ένας βασικός ρυθμιστής και διεγέρτης του άξονα HPG, μέσω της άμεσης δράσης της στο ΚΝΣ που οδηγεί στη ρύθμιση της έκκρισης της GnRH από τον υποθάλαμο.
Ωστόσο δεν υπάρχουν υποδοχείς λεπτίνης στους GnRH νευρώνες του ανθρώπου, γεγονός που υποδεικνύει την έμμεση δράση της λεπτίνης στον υποθάλαμο. Η δράση της λεπτίνης διαμεσολαβείται από νευρωνικούς μεσολαβητές όπως αMSH, AgRP και Neuropeptide–Y, που συντίθενται από νευρώνες που βρίσκονται στο τοξοειδή πυρήνα και προβάλλουν στους GnRH νευρώνες. Συγκεκριμένα αναστέλλει το νευροπεπτίδιο-Υ (NPY) και το agouti–related peptide (AgRP) ( ορεξιογόνα, αυξάνουν τη πρόσληψη τροφής) και διεγείρει τη Προοπιομελανοκορτίνη (POMC) η οποία με τη σειρά της ενεργοποιεί ανορεξιογόνους παράγοντες όπως την α-melanocyte stimulating hormone (αMSH) που αναστέλλουν τη πρόσληψη τροφής. Η λεπτίνη δρα και σε μία άλλη οικογένεια νευροπεπτιδίων που καλούνται kisspeptins, οι οποίες ρυθμίζουν την αναπραγωγική λειτουργία. Οι kiss1 νευρώνες του τοξοειδούς πυρήνα προβάλλουν στους GnRH νευρώνες και έχει προταθεί ότι παίζουν σημαντικό ρόλο στη διαμόρφωση των παλμών της GnRH.
Κλινικές παρατηρήσεις στον άνθρωπο
- Ασθενείς χωρίς το γονίδιο για τη λεπτίνη ή μη λειτουργικούς υποδοχείς της λεπτίνης δεν επιτυγχάνουν την εφηβική ωρίμανση και έχουν χαμηλάεπίπεδα LH, FSH ορού.
- Για την έναρξη της εφηβείας και τη συνέχιση των εμμηνορρυσιακών κύκλων είναι απαραίτητο ένα ελάχιστο όριο λεπτίνης.
- Μεταλλάξεις των γονιδίων της λεπτίνης και του υποδοχέα της έχει αποδειχθεί ότι είναι υπεύθυνες για υπογοναδοτροπικό υπογοναδισμό
- Ασθενείς που πάσχουν από νευρογενή ανορεξία εμφανίζουν δραματικά μειωμένη συγκέντρωση λεπτίνης στον ορό και συνήθως παρουσιάζουν κεντρική αμηνόρροια
- Η λειτουργία του γοναδοτροπικού άξονα μπορεί να αποκατασταθεί μετά από θεραπεία με ανασυνδυασμένη ανθρώπινη λεπτίνη σε περίπτωση μεταλλάξεων του γονιδίου της λεπτίνης.
Δράσεις λεπτίνης στα γυναικεία αναπαραγωγικά όργανα
Στους ανθρώπους υποδοχείς της λεπτίνης είναι παρόντες στα προ-ωοθυλακιορηκτικά ωοθυλάκια, στα κύτταρα θήκης, στα κοκκιώδη κύτταρα και τα ωοκύτταρα. Η λεπτίνη και οι υποδοχείς της εκφράζονται επίσης στο ενδομήτριο υποδηλώνοντας μια αυτοκρινική/ παρακρινική δράση και ένα ρόλο κατά την εμφύτευση του εμβρύου. χαμηλή έκφραση της λεπτίνης έχει αναφερθεί σε ασθενείς με αποτυχίες εμφύτευσης ή αποβολές, υπογραμμίζοντας το πιθανό ρόλο των υποδοχέων λεπτίνης στη λειτουργία του ενδομητρίου. Υψηλά επίπεδα λεπτίνης στις ωοθήκες μπορεί να καταστείλουν τη παραγωγή οιστραδιόλης, να εμπλακεί έτσι η λεπτίνη στην ανάπτυξη των ωοθυλακίων και την ωρίμανση των ωοκυττάρων δημιουργώντας έτσι τη προδιάθεση για έλλειψη ωορρηξίας. Για το λόγο αυτό σε καταστάσεις που συνοδεύονται με περίσσεια αποθηκών ενέργειας ή μεταβολικών διαταραχών (παχυσαρκία, PCOS) η λεπτίνη έχει ανασταλτική λειτουργία στις γονάδες. Από την άλλη στην υποθρεψία (διατροφικές διαταραχές, αμηνόρροια προκαλούμενη από υπερβολική άσκηση, λειτουργική υποθαλαμική αμηνόρροια) η έλλειψη λεπτίνης προκαλεί δυσλειτουργία στον άξονα HPG, αυξάνοντας έτσι τη πιθανότητα η αντίσταση στη λεπτίνη ή έλλειψη αυτής να είναι υπέθυνες για τις ανωμαλίες στην αναπαραγωγή που συνοδεύουν αυτές τις παθοφυσιολογικές καταστάσεις. Επιπλέον ο LEPR και το mRNA της λεπτίνης εκφράζοναται ειδικά στο στάδιο της βλαστοκύστης έχοντας ρόλο στην επικοινωνία βλαστοκύστης-ενδομητρίου.
Η λεπτίνη και οι υποδοχείς της επίσης βρίσκονται στη συγκυτιοτροφοβλάστη του πλακούντα υποστηρίζοντας ότι μπορεί να λειτουργεί με παρακρινή ή αυτοκρινή τρόπο στη λειτουργία του πλακούντα. Επίσης προηγούμενες μελέτες απέδειξαν τις αλληλεπιδράσεις μεταξύ λεπτίνης και ορμονών του πλακούντα αποδεικνύοντας έτσι ότι η λεπτίνη λειτουργεί σαν ρυθμιστής σε ένα βαθμό στις ενδοκρινικές λειτουργίες του πλακούντα. Η λεπτίνη διεγείρει το μονοπάτι σηματοδότησης της κινάσης JAK–STAT, μέσω εναργοποίησης της JAK2-STAT3 το οποίο φαίνεται να σχετίζεται με την ανάπτυξη της τροφοβλάστης. Η μεταβίβαση του σήματος μέσω μονοπατιών που περιλαμβάνουν τη κινάση της πρωτεΐνης ενεργοποιούμενης από μιτογόνα (MAPK) (μεσολαβεί στο πολλαπλασιασμό των κυττάρων) καθώς και μέσω του PI3K (ρυθμίζει τη διαφοροποίηση και το πολλαπλασιασμό στη τροφοβλάστη), έχει βρεθεί ότι σηματοδοτούν μονοπάτια που ενεργοποιούνται ως απάντηση στη λεπτίνη. Έτσι, καθώς τα κύτταρα της τροφοβλάστης παράγουν τοπικά λεπτίνη, αυτή προσδένεται σε υποδοχείς στο πλακούντα επηρεάζοντας τοπικά ή περιφερικά με τη δράση της. Συγκεκριμένα η πλακουντιακή λεπτίνη διεγείρει τη παραγωγή της χοριακής γοναδοτροπίνης hCG στα τροφοβλαστικά κύτταρα και αυξάνει τη σύνθεση των μεταλλοπρωτεϊνασών (MMP-2 and MMP-9). Ακόμη η λεπτίνη είναι ένας τροφικός και μιτογόνος παράγοντας για τα τροφοβλαστικά κύτταρα καταστέλλοντας την απόπτωση και επάγοντας τον πολλαπλασιασμό τους μέσω της ενεργοποίησης των JAK–STAT, MAPK, και PI3K. Η λεπτίνη συμβάλλει στην αγγειογένεση και ανοσορύθμιση μέσω του αυξητικού παράγοντα του ενδοθηλίου (VEGF) και του υποδοχέα του VEGF–R2 επάγοντας τη νεοαγγειογένεση στο πλακούντα. Η ανοσορύθμιση γίνεται μέσω ρύθμισης της ενεργοποίησης των NK κυττάρων , τα οποία παράγουν αγγειογόνους παράγοντες ,όπως η αγγειοποιητίνη-1 (Ang-1), Ang-2, και VEGF–C.
Αδιπονεκτίνη
H αδιπονεκτίνη είναι μία πρωτεϊνη 244 αμινοξέων που παράγεται κυρίως από το λευκό λιπώδη ιστό αλλά βρίσκεται και σε άλλους ιστούς όπως οι σκελετικοί μυς, τα οστά, ο υποθάλαμος, η υπόφυση, η μήτρα, οι ωοθήκες. Η έκφραση της αδιπονεκτίνης στα αναπαραγωγικά όργανα πολλών ζώων συμπεριλαμβανομένου του ανθρώπου υποδηλώνει την εμπλοκή της στις λειτουργίες του αναπαραγωγικού συστήματος.
Παρότι η αδιπονεκτίνη παράγεται κυρίως από το λευκό λιπώδη ιστό, η συγκέντρωσή της στον ορό είναι αντιστρόφως ανάλογη με το δείκτη μάζας σώματος και τη συνολική μάζα του λευκού λιπώδους ιστού. Τα επίπεδα της αδιπονεκτίνης είναι μικρότερα στα παχύσαρκα άτομα αλλά αυξάνονται με απώλεια βάρους. Η συγκέντρωσή της στο πλάσμα εξαρτάται από το φύλο (σεξουαλικός διμορφισμός). Οι γυναίκες έχουν 2-3 φορές υψηλότερα επίπεδα αδιπονεκτίνης από τους άνδρες.
Είναι γνωστή για την επίδρασή της στη βελτίωση της ευαισθησίας στην ινσουλίνη, στη καταστολή του κυτταρικού θανάτου, συμμετέχει στο μεταβολισμό των λιπιδίων και των υδατάνθράκων και στη ρύθμιση διαφόρων διεργασιών όπως η ενεργειακή ομοιόσταση (στο ήπαρ αναστέλλει τη γλυκονεογένεση, στους σκελετικούς μυς αυξάνει την οξείδωση των λιπαρών οξέων, στα παγκρεατικά κύτταρα και τα μυοκαρδιακά κύτταρα λειτουργεί ως αντι-λιποτοξικός παράγοντας, κυρίως επιδρά στα σφιγγολιπίδια) και η αγγειοδιαστολή. Η αδιπονεκτίνη είναι γνωστή για τις αντιφλεγμονώδεις ιδιότητές της. Φαίνεται να έχει ένα κύριο ρόλο στη παθοφυσιολογία της παχυσαρκίας, του ΣΔΤ2 και στη στεφανιαία νόσο.
Η αδιπονεκτίνη εκκρίνεται από το λιπώδη ιστό σα τριμερής μορφή χαμηλού μοριακού βάρους (LMV), σαν εξαμερής μορφή (συνδυασμός 2 τριμερών) μέσου μοριακού βάρους (MMW) και σαν πολυμερής μορφή υψηλού μοριακού βάρους (HMW). Οι βιολογικές της δράσεις ποικίλουν ανάλογα με τη διαφορετική δομή της και τον ιστό που δρα. Έχουν ταυτοποιηθεί τρεις υποδοχείς για την αδιπονεκτίνη AdipoR1, AdipoR2 και η T–cadherin. Η έκφραση AdipoRs επιβεβαιώθηκε σε όλες τις δομές του άξονα υποθαλάμου-υπόφυσης-γονάδες. Αντίθετα η T–cadherin φαίνεται ότι επιδρά μόνο σαν μια δεσμευτική πρωτεΐνη για την αδιπονεκτίνη.
Αδιπονεκτίνη – HPG
Η έκφραση των υποδοχέων της αδιπονεκτίνης έχει επιβεβαιωθεί στον ανθρώπινο υποθάλαμο, όπου εμπλέκεται στη ρύθμιση έκκρισης GnRH, αναστέλλοντάς τη. Η παρουσία της αδιπονεκτίνης και στην υπόφυση, ειδικά στα γοναδοτρόπα κύτταρα, και η επίδρασή της στην απελευθέρωση της LH και FSH, υποδεικνύει το πιθανό ρόλο της αδιπονεκτίνης ως μεταβολικού ρυθμιστή των αναπαραγωγικών λειτουργιών. Τα μέχρι τώρα δεδομένα υποδεικνύουν πιθανό ενδοκρινικό, παρακρινικό και αυτοκρινικό ρόλο τη αδιπονεκτίνης στη ρύθμιση της λειτουργίας των ωοθηκών. Η αδιπονεκτίνη φαίνεται ότι ρυθμίζει τη στεροειδογένεση από τα κοκκιώδη κύτταρα και τα κύτταρα θήκης, αν και τα ευρήματα δεν είναι σταθερά.
Η αδιπονεκτίνη μπορεί να είναι ένας παθοφυσιολογικός σύνδεσμος μεταξύ μεταβολικών διαταραχών (αντίσταση στην ινσουλίνη και παχυσαρκία) και διαταραχών γονιμότητας που απαντώνται σε ασθενείς με PCOS.
Επιπλέον, η αδιπονεκτίνη και οι υποδοχείς της εκφράζονται στο ανθρώπινο ενδομήτριο και έχει παρατηρηθεί μια ισχυρή έκφραση των υποδοχέων της στο ενδομήτριο κατά τη διάρκεια εμφύτευσης του εμβρύου. Μείωση της έκφρασης των AdipoR1 και AdipoR2 παρατηρήθηκε επίσης στο ενδομήτριο γυναικών με επαναλαμβανόμενες αποτυχίες εμφύτευσης σε σύγκριση με γόνιμες γυναίκες, υποδεικνύοντας ένα σημαντικό ρόλο της αδιπονεκτίνης στην ενδομήτρια υποδεκτικότητα και τη πιθανή συμβολή της σε αποτυχίες εμφύτευσης και απώλεια εγκυμοσύνης σε γυναίκες με μεταβολικές παθήσεις όπως η παχυσαρκία και PCOS.
Άλλες αδιποκίνες που σχετίζονται με την αναπαργωγή
Η Chemerin είναι μία προφλεγμονώδης αδιποκίνη που αρχικά παράγεται σαν μία πρωτεΐνη 163 αμινοξέων την pre–pro–chemerin, από την οποία με διάσπαση προκύπτει η αδρανής μορφή pro–chemerin, από την οποία με διαδοχικές πρωτεολυτικές διασπάσεις προκύπτουν διάφορες ισομορφές δραστικής chemerin. Η βιολογική δραστικότητα της chemerin εξαρτάται από το σημείο διάσπασης, το πρωτεολυτικό ένζυμο και το όργανο στόχος. Η chemerin και οι υποδοχείς της βρίσκονται σε όλο το σώμα και τα έως σήμερα ευρήματα δείχνουν ότι διαδραματίζει έναν πολύ-λειτουργικό ρόλο ως ρυθμιστής αρκετών φυσιολογικών διεργασιών, όπως ο έλεγχος της ΑΠ, η αγγειογένεση, η φλεγμονή, η ρύθμιση του ανοσοποητικού και του αναπαραγωγικού συστήματος. Η Chemerin ασκεί τις δράσεις της μέσω σύνδεσης με τρεις διαφορετικούς υποδοχείς: τον CMKLR1 (chemokine like receptor 1), τον GPR1 (G–protein–coupled receptor 1), CCRL2 (chemokine like receptor 2). Στους ανθρώπους, οι συγκεντρώσεις της Chemerin στο πλάσμα σχετίζονται με το σωματικό λίπος και είναι αυξημένες σε ασθενείς με παχυσαρκία και/ή ΣΔ και σε φλεγμονώδεις καταστάσεις. Επιπλέον λειτουργεί χημειοτακτικά στα κύτταρα του ανοσοποιητικού, προκαλεί βλάβη στα αγγεία, μπορεί να παίζει ρόλο στη γένεση των στρωματικών κυττάρων του λίπους, μπορεί να επηρεάζει την αντίσταση στην ινσουλίνη, αυξάνει την οστεοκλαστική δραστηριότητα, αυξάνει την αντίσταση στην ινσουλίνη στο μυϊκό ιστό.
Η Chemerin είναι μια βασική ορμόνη που συνδέει τις αναπαραγωγικές και μεταβολικές λειτουργίες. Μπορεί να παίζει έναν παρακρινό ή/και αυτοκρινό ρυθμιστικό ρόλο στις ωοθήκες. Επηρεάζοντας αρνητικά τη στεροειδογένεση και συμμετέχοντας στη παύση της ανάπτυξης των ωοθυλακίων με άντρο, η Chemerin φαίνεται να παίζει σημαντικό ρόλο στη παθολογική διαδικασία του PCOS. Έχει υποτεθεί ότι παίζει ρόλο στη πλακουντοποίηση και μπορεί να έχει ένα ρόλο στην εμβρυική ανάπτυξη.
Η Resistin είναι ένα προπεπτίδιο 108 αμινοξέων και σχηματίζει συμπλέγματα υψηλού και χαμηλού μοριακού βάρους. Οι δεσμοί δισουλφιδίου και μη-δισουλφιδίου παίζουν επίσης σημαντικό ρόλο στο σχηματισμό μορφών διμερούς, τριμερούς και εξαμερούς κυκλοφορούσας Resistin. Τα λιποκύτταρα δεν είναι η κύρια πηγή της κυκλοφορούσας Resistin στους ανθρώπους. Τα μονοπύρηνα κύτταρα περιφερικού αίματος, τα μακροφάγα κύτταρα και τα κύτταρα μυελού των οστών είναι η κύρια πηγή. Η Resistin επηρεάζει λειτουργικά το μεταβολισμό της γλυκόζης και έχει συσχετιστεί στους ανθρώπους με χρόνιες φλεγμονώδεις και αυτοάνοσες ασθένειες. Αναφορές δείχνουν ότι η Resistin εκφράζεται στον άξονα υποθάλαμος-υπόφυση-γονάδες και ρυθμίζει διάφορες αναπαραγωγικές λειτουργίες. Τα αποτελέσματα σχετικά με τα επίπεδα της Resistin σε ασθενείς με PCOS εξακολουθούν να είναι αμφιλεγόμενα. Φαίνεται να είναι παρούσα στο πλακούντα και μπορεί να συμβάλλει στον έλεγχο της αγγειακής ανάπτυξης του πλακούντα. Η έκφραση της Resistin στο πλακούντα είναι σημαντικά υψηλότερη στο τελευταίο τρίμηνο από ότι στο πρώτο τρίμηνο και μπορεί να εμπλέκεται στην υπερβολική φλεγμονώδη απόκριση της μητέρας που σχετίζεται με τη παθογένεια της προεκλαμψίας.
Η Omentin, που ονομάζεται επίσης και Omentin-1, είναι μια νέα πρωτείνη που παράγεται κυρίως από το σπλαχνικό λίπος στους ανθρώπους. Η έκφραση της Omentin-1 έχει επίσης ανιχνευθεί στους ανθρώπους και σε άλλους ιστούς σε χαμηλά επίπεδα, μεταξύ των οποίων και οι αναπαραγωγικοί ιστοί. Η Omentin-1 αυξάνει τη δράση της ινσουλίνης, σχετίζεται αντιστρόφως με τη παχυσαρκία και αυξάνεται με την απώλεια βάρους. Ευρήματα δείχνουν ότι η Omentin-1 μπορεί να επηρεάζει την έκκριση ορμονών που ρυθμίζουν την ωοθηκική και εμμηνορρυσιακή λειτουργία ή να επηρεάζει τους υποδοχείς αυτών των ορμονών. Τα επίπεδα Omentin-1 πλάσματος είναι υψηλότερα στις γυναίκες από τους άντρες και μειώνονται σε γυναίκες με PCOS σε σύγκριση με γυναίκες χωρίς PCOS και ίδιο ΒΜΙ. Η Omentin-1 έχει συνδεθεί με το μεταβολικό συνδρομο και το PCOS. Η Omentin-1 φαίνεται ότι μπορεί να εμπλέκεται στην ωοθυλακιογένεση και μπορεί να συμβάλει στη παθοφσιολογία του PCOS.
Η Visfatin είναι μια πρωτείνη 491 αμινοξέων που εκφράζεται σε διάφορους ιστούς, αλλά κυρίως στο σπλαχνικό λιπώδη ιστό. Η Visfatin παρουσιάζει μιμητικές δράσεις της ινσουλίνης. Ο υποδοχέας της είναι ακόμη άγνωστος καθώς και η εμπλεκόμενη οδός σηματοδότησης. Στα θηλαστικά η Visfatin ή το NAMPT υπάρχει σε δύο μορφές, την ενδοκυττάρια και την εξωκυττάρια (iNAMPT, eNAMPT). Ενώ η λειτουργία του iNAMPT έχει εδραιωθεί σταθερά ως ένα βιοσυνθετικό ένζυμο NAD και έχει σημαντικό ρόλο στα μιτοχόνδρια, η λειτουργία του eNAMPT είναι αμφιλεγόμενη. Η Visfatin δρα επίσης ως κυτταρικίνη που εμπλέκεται στο μεταβολισμό (παχυσαρκία, διαβήτης τύπου 2) και ανοσολογικές διαταραχές. Έχει βρεθεί ότι τα επίπεδα της Visfatin στον ορό μειώνονται σε γυναίκες με προεκλαμψία και μειώνονται περαιτέρω στη σοβαρή μορφή της νόσου. Παρότι στον άνθρωπο ο ακριβής αναπαραγωγικός ρόλος της Visfatin παραμένει αναμφισβητούμενος, αρκετές μελέτες έδειξαν ότι η visfatin στην ωοθήκη εμφανίζει προ-φλεγμονώδεις ιδιότητες και ανοσολογικές δράσεις, υποδεικνύοντας ένα πιθανό ρόλο στη παθογένεια του PCOS.
Η ανθρώπινη Apelin εντοπίζεται με τη μορφή της preproapelin (77αμινοξέα) που θα διασπαστεί από ενδοπεπτιδάσες και θα προκύψει η proapelin (55 αμινοξέα) και στη συνέχεια σε άλλες ενεργείς ισομορφές (36,17,13 και Pyr-13 αμινοξέα). Η Apelin εκφράζεται ευρέως σε διάφορους τύπους ιστών και όργανα (κεντρικό νευρικό σύστημα, υποθάλαμος, λιπώδης ιστός, σκελετικός μυς, πεπτικό σύστημα και ωοθήκες). Σηματοδοτεί μέσω του υποδοχέα εξαρτώμενου από G πρωτεΐνη (APLNR). Βελτιώνει την αντίσταση στη γλυκόζη και την ευαισθησία στην ινσουλίνη, συμβάλλει στην ομοιόσταση των βιολογικών υγρών, μπορεί να επηρεάζει τη μυϊκή μάζα, αυξάνει τη πρόσληψη γλυκόζης από τα κύτταρα του λιπώδους και του μυϊκού ιστού, αυξάνει τη θερμογένεση από το λιπώδη ιστό και την αγγειογένεση, αυξάνει τη κατανάλωση ενέργειας, τη λεμφαγγειογένεση, τη βιογένεση μιτοχονδρίων στο μυϊκό ιστό και την οξείδωση των λιπαρών οξέων, συμβάλλει στην ελάττωση του σωματικού βάρους, της ΑΠ, τέλος μπορεί να ελαττώσει τη φλεγμονή και την ηπατική στεάτωση. Τα έως τώρα ευρήματα υποδεικνύουν ένα ρόλο της Apelin στην ορμονική ρύθμιση της ωοθηκικής λειτουργίας και υποστηρίζουν τη πιθανή εμπλοκή της Apelin στις διαταραχές του άξονα υποθαλάμου-υπόφυσης-ωοθηκών και στην ωοθηλακιορρηκτική δυσλειτουργία που συνδέεται με το PCOS. Η Apelin εκφράζεται επιπλέον στον ανθρώπινο πλακούντα. Το σύστημα Apelin/APJ μπορεί να έχει ρόλο στη παθογένεια της προεκλαμψίας.
Συμπεράσματα
Ο λιπώδης ιστός και το κύριο συστατικό του, τα λιποκύτταρα, είναι απαραίτητα για την επιβίωση. Προστατεύουν το σώμα από από το τραύμα, παρέχουν τη κύρια πηγή αποθηκευμένης ενέργειας και επηρεάζουν μια πληθώρα φυσιολογικών λειτουργιών, συμπεριλαμβανομένης της αναπαραγωγής, μέσω μιας σειράς εκκρινόμενων προϊόντων, συλλογικά γνωστών ως αδιποκίνες. Είναι πλέον σαφές ότι ο λιπώδης ιστός επικοινωνεί με τον εγκέφαλο, τις γονάδες και τη μήτρα για να ρυθμίζει τις αναπαραγωγικές λειτουργίες μέσω αυτών των αδιποκινών και κατά συνέπεια οι αδιποκίνες συμμετέχουν στη εξήγηση ορισμένων αναπαραγωγικών διαταραχών. Αυτές οι αδιποκίνες έχουν ωφέλιμες ή ασκούν αρνητικές επιδράσεις στη γονιμότητα του ανθρώπου; Οι περισσότερες μελέτες έχουν γίνει σε in vitro κύτταρα των ωοθηκών και οι in vivo μελέτες είναι περιορισμένες, οπότε είναι δύσκολο να δοθεί απάντηση για ολόκληρο τον οργανισμό. Μερικές φορές τα δεδομένα in vitro είναι αντιφατικά, γεγονός που μπορεί να εξηγηθεί από διαφορές ανάλογα με το είδος, αλλά και από τη χρήση διαφορετικών συγκεντρώσεων των αδιποκινών ή/και διαφορετικού πειραματικού σχεδιασμού. Είναι ενδιαφέρον ότι η έκφραση των αδιποκινών στο πλάσμα ή και στους ιστούς μπορεί να σχετίζεται με διάφορες γυναικείες αναπαραγωγικές διαταραχές συμπεριλαμβανομένου του συνδρόμου PCOS, του διαβήτη κύησης, της προεκλαμψίας, της ενδομήτριας καθυστέρησης της ανάπτυξης του εμβρύου. Απαιτούνται πρόσθετες μελέτες για τη καλύτερη κατανόηση του ρόλου και του μοριακού μηχανισμού των αδιποκινών στον έλεγχο της γονιμότητας προκειμένου να χρησιμοποιηθούν ενδεχομένως ως προγνωστικοί δείκτες ή/και θεραπευτικοί στόχοι σε διάφορες αναπαραγωγικές διαταραχές.
Βιβλιογραφία
- Biochemistry of adipose tissue: an endocrine organ
Arch Med Sci 2013; 9, 2: 191-200 DOI: 10.5114/aoms.2013.33181 Copyright © 2013 Termedia & Banach
- Role of leptin in female reproduction Clin Chem Lab Med 2015; 53(1): 15–28
Antonio Pérez-Pérez, Flora Sánchez-Jiménez, Julieta Maymó, José L. Dueñas, Cecilia Varone and Víctor Sánchez-Margalet*
DOI 10.1515/cclm-2014-0387 Received April 8, 2014; accepted June 16, 2014; previously published online July 11, 2014
- The role of visfatin in the pathogenesis of gestational diabetes (GDM) Sandra Radzicka, Marek Pietryga, Rafał Iciek, Jacek Brązert Department of Obstetrics and Women Diseases, University of Medical Science, Poznań, Poland
Ginekologia Polska 2018, vol. 89, no. 9, 518–521 Copyright © 2018 Via Medica ISSN 0017–0011 DOI: 10.5603/GP.a2018.0088
- Adipocytokines: mediators linking adipose tissue, inflammation and immunity
DOI: 10.1038/nri1937
- Beyond adiponectin and leptin: adipose tissue-derived mediators of inter-organ communication
Jan-Bernd Funcke and Philipp E. Scherer1 Touchstone Diabetes Center, University of Texas Southwestern Medical Center, Dallas, TX ORCID IDs: 0000-0002-2596-3167 (J-B.F.); 0000-0003-0680-3392 (P.E.S.)
TrueMed-ForLivingMore
Κοινοποιήστε



Αρχές Βιοηθικής και Διαχείρισης των Ζώων στην Βιοϊατρική Έρευνα και την Κτηνιατρική Επιστήμη
Η παρούσα μελέτη, προσεγγίζοντας το ζήτημα των καινοτόμων θεραπευτικών σχημάτων επιχειρεί να αναδείξει το ευρύτερο πλαίσιο και τις αρχές στο πεδίο της βιοηθικής και διαχείρισης των ζώων στην βιοϊατρική έρευνα και την κτηνιατρική επιστήμη

Βήμα προς βήμα το θερμικό σοκ σε ένα βρέφος
Το θερμικό σοκ σε βρέφη είναι ταχύτατα εξελισσόμενο και δυνητικά θανατηφόρο.
Κάθε λεπτό καθυστέρησης αυξάνει τον κίνδυνο βλάβης ή θανάτου.
ΡΟΗ ΕΙΔΗΣΕΩΝ
Βρείτε μας στο Facebook και στο Instagram
| Επικοινωνία | Η ομάδα μας | Διαφημιστείτε στη truemed.gr| | Όροι χρήσης | Προσωπικά δεδομένα | Copyright©Truemed | |Για περισσότερη ζωή |
Designed – Developed by Premiumweb.gr

© 2019 TrueMed Media. All rights reserved. Our website services, content, and products are for informational purposes only. TrueMed Media does not provide medical advice, diagnosis, or treatment.
Το λίπος… απλά αποθήκη ενέργειας; (Ο ρόλος του στον οργανισμό)
![]() 23-11-2020
23-11-2020
![]() Άννα Μαντά
Άννα Μαντά

Ο λιπώδης ιστός ο οποίος κάποτε θεωρείτο αδρανές όργανο αποθήκευσης ενέργειας που παρέχει μόνωση από το κρύο, αναγνωρίζεται πλέον ως ένα δυναμικό ενδοκρινικό σύστημα.
Αποτελείται από πολλά κύτταρα συμπεριλαμβανομένων των λιποκυττάρων, των προ-λιποκυττάρων, των ενδοθηλιακών κυττάρων, των μονοκυττάρων, των μακροφάγων και του ινοβλαστικού συνδετικού ιστού.

Η λιπογένεση αναφέρεται στη διαφοροποίηση των προ-αδιποκυττάρων σε ώριμα λιποκύτταρα με σκοπό την ανάπτυξη του λιπώδους ιστού, γεγονός που διαφοροποιείται ανάλογα με το φύλο και την ηλικία. Τα λιποκύτταρα διαφοροποιούνται από αστεροειδή και ατρακτοειδή πρόδρομα κύτταρα μεσεγχυματικής προέλευσης.
Τα προ-αδιποκύτταρα στο λιπώδη ιστό μπορούν να διαφοροποιηθούν σε ώριμα αδιποκύτταρα κατά τη διάρκεια της ζωής, επιτρέποντας έτσι την υπερπλασία του λιπώδους ιστού όταν οι ανάγκες για αποθήκευση ενέργειας αυξάνονται. Επιπλέον τα ώριμα λιποκύτταρα μπορούν να αυξηθούν σε μέγεθος σε καταστάσεις όπως η υπερβολική θρέψη με αποτέλεσμα να γίνονται υπερτροφικά. Τελικά ο αριθμός των λιποκυττάρων και η μορφολογία τους ρυθμίζεται από βιοχημικές διαδικασίες όπως η εστεροποίηση, λιπόλυση και διαφοροποίηση των προ-αδιποκυττάρων, ως απάντηση σε αλλαγές της ενεργειακής ισορροπίας.
Υπάρχουν δύο τύποι ώριμων λιποκυττάρων στα θηλαστικά: τα καφέ και τα λευκά λιποκύτταρα
Τα καφέ λιποκύτταρα είναι πιο άφθονα στη παιδική ηλικία, αλλά αντιπροσωπεύονται ελάχιστα στους ενήλικες, εμπλέκονται στη βασική παραγωγή θερμότητας, ενώ τα λευκά χρησιμεύουν ως μακροπρόθεσμη δεξαμενή καυσίμων.
Γυναίκες και άνδρες παρουσιάζουν διμορφική σύνθεση του σωματικού τους λίπους, με τους άνδρες να έχουν κεντρική ή κοιλιακή παχυσαρκία, ενώ οι γυναίκες έχουν περισσότερο λίπος στη περιοχή των μηρών και των γλουτών.
Τα λευκά λιποκύτταρα παράγουν πολυάριθμα ενδοκρινικά, παρακρινικά και νευροενδοκρινικά σήματα μέσω της παραγωγής αδιποκινών.
Οι αδιποκίνες περιλαμβάνουν οποιαδήποτε ουσία που απελευθερώνεται από το λιπώδη ιστό, είτε από τα λιποκύτταρα, διηθητικά μακροφάγα, στρωματικά κύτταρα ή άλλα μέρη του λιπώδους ιστού (συνδετικός ιστός και αιμοφόρα αγγεία).
Αυτές οι ουσίες περιλαμβάνουν κυτταροκίνες, αυξητικούς παράγοντες, χημειοκίνες, παράγοντες συμπληρώματος και πρωτεΐνες που εμπλέκονται στην αγγειακή αιμόσταση, στη ρύθμιση της αρτηριακής πίεσης, το μεταβολισμό των λιπιδίων, την ομοιοστασία της γλυκόζης, στη φλεγμονή, στην αγγειογένεση και στην αναπαραγωγή
Οι ποσότητες των αδιποκινών μπορεί να ποικίλουν ανάλογα με τη μεταβολική κατάσταση (πχ. Νοσογόνος παχυσαρκία), το διαμέρισμα του λίπους (σπαλχνικό,υποδόριο) και την ανάπτυξη των κυττάρων (προλιποκύτταρα, ώριμα λιποκύτταρα).
Ορισμένες αδιποκίνες απελευθερώνονται σε σημαντικές ποσότητες στη κυκλοφορία (πχ λεπτίνη, αδιπονεκτίνη), ενώ άλλες όπως ο TNF–a, παραμένουν κυρίως εντοπισμένες στο λιπώδη ιστό και λειτουργούν ως παρακρινικοί ή αυτοκρινικοί ρυθμιστές.
Ο αριθμός των αδιποκινών εξελίσσεται (>600 πιθανοί διαμεσολαβητές σηματοδότησης κυττάρων) και αρκετές αδιποκίνες αναγνωρίζονται σήμερα ως πιθανοί μεσολαβητές της αναπαραγωγικής υγείας και των αναπαραγωγικών διαταραχών.

Η λεπτίνη είναι μία ορμόνη που αποτελείται από 167 αμινοξέα και συντίθεται στο λευκό λιπώδη ιστό, συμμετέχει στη ρύθμιση πρόσληψης τροφής και ενεργειακής ομοιόστασης ενεργώντας στο ΚΝΣ. Η λεπτίνη και το γονίδιό της (obesity gene) ανακαλύφθηκαν το 1994. Η έκφραση του γονιδίου της λεπτίνης ρυθμίζεται από μία ποικιλία ορμονών, κυτταροκινών και αυξητικών παραγόντων. Τα οιστρογόνα επάγουν, ενώ τα ανδρογόνα καταστέλλουν τη παραγωγή λεπτίνης, παρέχοντας μία εξήγηση για το σεξουαλικό διμορφισμό σε επίπεδα λεπτίνης στον ορό.

Οι μεταλλάξεις σε αυτό το γονίδιο προκαλούν νοσογόνο παχυσαρκία και διαβήτη σε ανθρώπους και ζώα. Αν και η λεπτίνη είχε αρχικά θεωρηθεί οτί εκφράζεται αποκλειστικά στο λευκό λιπώδη ιστό, μεταγενέστερες αναφορές έδειξαν ότι η λεπτίνη εκφράζεται και σε άλλες περιοχές, όπως ο υποθάλαμος, η υπόφυση, το γαστρικό επιθήλιο, οι σκελετικοί μυς, ο πλακούντας, ο μαστός και οι γονάδες.
Η λεπτίνη εκκρίνεται με παλμικό τρόπο με σημαντική ημερήσια διακύμανση (χαμηλότερα επίπεδα στα μέσα του απογεύματος και υψηλότερα επίπεδα τα μεσάνυκτα). Η στάθμη της στον ορό σχετίζεται με τη ποσότητα και τη κατανομή της μάζας του σωματικού λίπους, παρέχοντας ένα περιφερειακό σήμα στο ΚΝΣ σχετικά με την επάρκεια της διατροφικής κατάστασης. Επιπλέον η ορμόνη εμπλέκεται στον έλεγχο πολλών φυσιολογικών λειτουργιών, όπως η ανάπτυξη, ο μεταβολισμός και η αναπαραγωγή.
Υποδοχείς λεπτίνης
Οι υποδοχείς λεπτίνης (ObRs) ανήκουν στην οικογένεια υποδοχέων κυταροκίνης και εντοπίζονται στο ΚΝΣ και σε περιφερικούς ιστούς. Υπάρχουν 6 ισομορφές του υποδοχέα λεπτίνης (4 μορφές έχουν βρεθεί στον άνθρωπο), οι οποίες έχουν μια εξωκυττάρια περιοχή και είτε δεν έχουν τη διαμεμβρανική περιοχή (ObRe, ισομορφή που αντιπροσωπεύει τη κυκλοφορούσα μορφή του Ob–R)είτε έχουν διαφορετικά μήκη της ενδοκυτταρικής περιοχής (Οb–Ra,bc,d,f). H λεπτίνη κυκλοφορεί στα βιολογικά υγρά τόσο ως ελεύθερη όσο και σε μορφή που δεσμεύεται με τη διαλυτή ισομορφή του υποδοχέα της (Οb–Re).
Οι υποδοχείς της λεπτίνης εκφράζονται σε όλο το σώμα, συμπεριλαμβανομένου του ΚΝΣ, όπου η λεπτίνη δρα για τη ρύθμιση της νευροενδοκρινικής λειτουργίας, της διατροφικής συμπεριφοράς και της ενεργειακής δαπάνης. Η λεπτίνη εκτελεί τη δράση της μέσω του υποδοχέα της, ο οποίος με τη σειρά του ενεργοποιεί πολλές ενδοκυτταρικές οδούς σηματοδότησης.
Ακόμη οι υποδοχείς της λεπτίνης (ObRs) έχουν ταυτοποιηθεί στον υποθάλαμο, στα γοναδοτρόπα κύτταρα της πρόσθιας υπόφυσης, στα κοκκιώδη κύτταρα, στα κύτταρα της θήκης και στο ενδομήτριο. Αυτή η πολυεστιακή έκφραση της λεπτίνης, καθώς και η πυκνή παρουσία Ob–Rs σε όλα τα επίπεδα του άξονα υποθαλάμου-υπόφυση-γονάδες (HPG), υποδηλώνει ότι η ρύθμιση της αναπαραγωγής μέσω της λεπτίνης περιλαμβάνει ένα περίπλοκο δίκτυο αλληλεπιδράσεων σε πολλαπλά επίπεδα για να ρυθμίσει τον άξονα HPG με παρακρινικό ή/και ενδοκρινικό τρόπο.
Τα παχύσαρκα άτομα παρουσιάζουν υψηλά επίπεδα έκφρασης της λεπτίνης στο λιπώδη ιστό και έχουν αυξημένα επίπεδα λεπτίνης στη κυκλοφορία, όμως αυτά τα επίπεδα αποτυγχάνουν να μειώσουν τη περίσσεια του λίπους, εμφανίζοντας αντίσταση στη λεπτίνη. H λεπτίνη αυξάνεται από τα γλυκοκορτικοειδή, στην οξεία λοίμωξη και από προ-φλεγμονώδεις κυτταροκίνες. Αντίθετα η έκθεση στο κρύο, η αδρενεργική διέγερση, η αυξητική ορμόνη, οι ορμόνες του θυρεοειδούς, η μελατονίνη, το κάπνισμα και οι θειαζολιδινεδιόνες μειώνουν τα επίπεδα λεπτίνης. Τα επίπεδά της είναι υψηλότερα στις γυναίκες σε σύγκριση με τους άνδρες, εν μέρη λόγω της αναστολής της από τα ανδρογόνα, τη διέγερσή της από τα οιστρογόνα και λόγω των διαφορών στην έκφρασή της ανάμεσα στα δύο φύλα. Επίσης η λεπτίνη συντίθεται σε μεγαλύτερο ποσοστό στο υποδόριο λίπος παρά στο σπλαχνικό, γεγονός που εξηγεί και τα υψηλότερα επίπεδά της στις γυναίκες λόγω αυξημένου υποδόριου λίπους.
Στη περίπτωση της γυναικείας υπογονιμότητας, η λεπτίνη είναι ένας βασικός ρυθμιστής και διεγέρτης του άξονα HPG, μέσω της άμεσης δράσης της στο ΚΝΣ που οδηγεί στη ρύθμιση της έκκρισης της GnRH από τον υποθάλαμο.
Ωστόσο δεν υπάρχουν υποδοχείς λεπτίνης στους GnRH νευρώνες του ανθρώπου, γεγονός που υποδεικνύει την έμμεση δράση της λεπτίνης στον υποθάλαμο. Η δράση της λεπτίνης διαμεσολαβείται από νευρωνικούς μεσολαβητές όπως αMSH, AgRP και Neuropeptide–Y, που συντίθενται από νευρώνες που βρίσκονται στο τοξοειδή πυρήνα και προβάλλουν στους GnRH νευρώνες. Συγκεκριμένα αναστέλλει το νευροπεπτίδιο-Υ (NPY) και το agouti–related peptide (AgRP) ( ορεξιογόνα, αυξάνουν τη πρόσληψη τροφής) και διεγείρει τη Προοπιομελανοκορτίνη (POMC) η οποία με τη σειρά της ενεργοποιεί ανορεξιογόνους παράγοντες όπως την α-melanocyte stimulating hormone (αMSH) που αναστέλλουν τη πρόσληψη τροφής. Η λεπτίνη δρα και σε μία άλλη οικογένεια νευροπεπτιδίων που καλούνται kisspeptins, οι οποίες ρυθμίζουν την αναπραγωγική λειτουργία. Οι kiss1 νευρώνες του τοξοειδούς πυρήνα προβάλλουν στους GnRH νευρώνες και έχει προταθεί ότι παίζουν σημαντικό ρόλο στη διαμόρφωση των παλμών της GnRH.
Κλινικές παρατηρήσεις στον άνθρωπο
- Ασθενείς χωρίς το γονίδιο για τη λεπτίνη ή μη λειτουργικούς υποδοχείς της λεπτίνης δεν επιτυγχάνουν την εφηβική ωρίμανση και έχουν χαμηλάεπίπεδα LH, FSH ορού.
- Για την έναρξη της εφηβείας και τη συνέχιση των εμμηνορρυσιακών κύκλων είναι απαραίτητο ένα ελάχιστο όριο λεπτίνης.
- Μεταλλάξεις των γονιδίων της λεπτίνης και του υποδοχέα της έχει αποδειχθεί ότι είναι υπεύθυνες για υπογοναδοτροπικό υπογοναδισμό
- Ασθενείς που πάσχουν από νευρογενή ανορεξία εμφανίζουν δραματικά μειωμένη συγκέντρωση λεπτίνης στον ορό και συνήθως παρουσιάζουν κεντρική αμηνόρροια
- Η λειτουργία του γοναδοτροπικού άξονα μπορεί να αποκατασταθεί μετά από θεραπεία με ανασυνδυασμένη ανθρώπινη λεπτίνη σε περίπτωση μεταλλάξεων του γονιδίου της λεπτίνης.
Δράσεις λεπτίνης στα γυναικεία αναπαραγωγικά όργανα
Στους ανθρώπους υποδοχείς της λεπτίνης είναι παρόντες στα προ-ωοθυλακιορηκτικά ωοθυλάκια, στα κύτταρα θήκης, στα κοκκιώδη κύτταρα και τα ωοκύτταρα. Η λεπτίνη και οι υποδοχείς της εκφράζονται επίσης στο ενδομήτριο υποδηλώνοντας μια αυτοκρινική/ παρακρινική δράση και ένα ρόλο κατά την εμφύτευση του εμβρύου. χαμηλή έκφραση της λεπτίνης έχει αναφερθεί σε ασθενείς με αποτυχίες εμφύτευσης ή αποβολές, υπογραμμίζοντας το πιθανό ρόλο των υποδοχέων λεπτίνης στη λειτουργία του ενδομητρίου. Υψηλά επίπεδα λεπτίνης στις ωοθήκες μπορεί να καταστείλουν τη παραγωγή οιστραδιόλης, να εμπλακεί έτσι η λεπτίνη στην ανάπτυξη των ωοθυλακίων και την ωρίμανση των ωοκυττάρων δημιουργώντας έτσι τη προδιάθεση για έλλειψη ωορρηξίας. Για το λόγο αυτό σε καταστάσεις που συνοδεύονται με περίσσεια αποθηκών ενέργειας ή μεταβολικών διαταραχών (παχυσαρκία, PCOS) η λεπτίνη έχει ανασταλτική λειτουργία στις γονάδες. Από την άλλη στην υποθρεψία (διατροφικές διαταραχές, αμηνόρροια προκαλούμενη από υπερβολική άσκηση, λειτουργική υποθαλαμική αμηνόρροια) η έλλειψη λεπτίνης προκαλεί δυσλειτουργία στον άξονα HPG, αυξάνοντας έτσι τη πιθανότητα η αντίσταση στη λεπτίνη ή έλλειψη αυτής να είναι υπέθυνες για τις ανωμαλίες στην αναπαραγωγή που συνοδεύουν αυτές τις παθοφυσιολογικές καταστάσεις. Επιπλέον ο LEPR και το mRNA της λεπτίνης εκφράζοναται ειδικά στο στάδιο της βλαστοκύστης έχοντας ρόλο στην επικοινωνία βλαστοκύστης-ενδομητρίου.
Η λεπτίνη και οι υποδοχείς της επίσης βρίσκονται στη συγκυτιοτροφοβλάστη του πλακούντα υποστηρίζοντας ότι μπορεί να λειτουργεί με παρακρινή ή αυτοκρινή τρόπο στη λειτουργία του πλακούντα. Επίσης προηγούμενες μελέτες απέδειξαν τις αλληλεπιδράσεις μεταξύ λεπτίνης και ορμονών του πλακούντα αποδεικνύοντας έτσι ότι η λεπτίνη λειτουργεί σαν ρυθμιστής σε ένα βαθμό στις ενδοκρινικές λειτουργίες του πλακούντα. Η λεπτίνη διεγείρει το μονοπάτι σηματοδότησης της κινάσης JAK–STAT, μέσω εναργοποίησης της JAK2-STAT3 το οποίο φαίνεται να σχετίζεται με την ανάπτυξη της τροφοβλάστης. Η μεταβίβαση του σήματος μέσω μονοπατιών που περιλαμβάνουν τη κινάση της πρωτεΐνης ενεργοποιούμενης από μιτογόνα (MAPK) (μεσολαβεί στο πολλαπλασιασμό των κυττάρων) καθώς και μέσω του PI3K (ρυθμίζει τη διαφοροποίηση και το πολλαπλασιασμό στη τροφοβλάστη), έχει βρεθεί ότι σηματοδοτούν μονοπάτια που ενεργοποιούνται ως απάντηση στη λεπτίνη. Έτσι, καθώς τα κύτταρα της τροφοβλάστης παράγουν τοπικά λεπτίνη, αυτή προσδένεται σε υποδοχείς στο πλακούντα επηρεάζοντας τοπικά ή περιφερικά με τη δράση της. Συγκεκριμένα η πλακουντιακή λεπτίνη διεγείρει τη παραγωγή της χοριακής γοναδοτροπίνης hCG στα τροφοβλαστικά κύτταρα και αυξάνει τη σύνθεση των μεταλλοπρωτεϊνασών (MMP-2 and MMP-9). Ακόμη η λεπτίνη είναι ένας τροφικός και μιτογόνος παράγοντας για τα τροφοβλαστικά κύτταρα καταστέλλοντας την απόπτωση και επάγοντας τον πολλαπλασιασμό τους μέσω της ενεργοποίησης των JAK–STAT, MAPK, και PI3K. Η λεπτίνη συμβάλλει στην αγγειογένεση και ανοσορύθμιση μέσω του αυξητικού παράγοντα του ενδοθηλίου (VEGF) και του υποδοχέα του VEGF–R2 επάγοντας τη νεοαγγειογένεση στο πλακούντα. Η ανοσορύθμιση γίνεται μέσω ρύθμισης της ενεργοποίησης των NK κυττάρων , τα οποία παράγουν αγγειογόνους παράγοντες ,όπως η αγγειοποιητίνη-1 (Ang-1), Ang-2, και VEGF–C.
Αδιπονεκτίνη
H αδιπονεκτίνη είναι μία πρωτεϊνη 244 αμινοξέων που παράγεται κυρίως από το λευκό λιπώδη ιστό αλλά βρίσκεται και σε άλλους ιστούς όπως οι σκελετικοί μυς, τα οστά, ο υποθάλαμος, η υπόφυση, η μήτρα, οι ωοθήκες. Η έκφραση της αδιπονεκτίνης στα αναπαραγωγικά όργανα πολλών ζώων συμπεριλαμβανομένου του ανθρώπου υποδηλώνει την εμπλοκή της στις λειτουργίες του αναπαραγωγικού συστήματος.
Παρότι η αδιπονεκτίνη παράγεται κυρίως από το λευκό λιπώδη ιστό, η συγκέντρωσή της στον ορό είναι αντιστρόφως ανάλογη με το δείκτη μάζας σώματος και τη συνολική μάζα του λευκού λιπώδους ιστού. Τα επίπεδα της αδιπονεκτίνης είναι μικρότερα στα παχύσαρκα άτομα αλλά αυξάνονται με απώλεια βάρους. Η συγκέντρωσή της στο πλάσμα εξαρτάται από το φύλο (σεξουαλικός διμορφισμός). Οι γυναίκες έχουν 2-3 φορές υψηλότερα επίπεδα αδιπονεκτίνης από τους άνδρες.
Είναι γνωστή για την επίδρασή της στη βελτίωση της ευαισθησίας στην ινσουλίνη, στη καταστολή του κυτταρικού θανάτου, συμμετέχει στο μεταβολισμό των λιπιδίων και των υδατάνθράκων και στη ρύθμιση διαφόρων διεργασιών όπως η ενεργειακή ομοιόσταση (στο ήπαρ αναστέλλει τη γλυκονεογένεση, στους σκελετικούς μυς αυξάνει την οξείδωση των λιπαρών οξέων, στα παγκρεατικά κύτταρα και τα μυοκαρδιακά κύτταρα λειτουργεί ως αντι-λιποτοξικός παράγοντας, κυρίως επιδρά στα σφιγγολιπίδια) και η αγγειοδιαστολή. Η αδιπονεκτίνη είναι γνωστή για τις αντιφλεγμονώδεις ιδιότητές της. Φαίνεται να έχει ένα κύριο ρόλο στη παθοφυσιολογία της παχυσαρκίας, του ΣΔΤ2 και στη στεφανιαία νόσο.
Η αδιπονεκτίνη εκκρίνεται από το λιπώδη ιστό σα τριμερής μορφή χαμηλού μοριακού βάρους (LMV), σαν εξαμερής μορφή (συνδυασμός 2 τριμερών) μέσου μοριακού βάρους (MMW) και σαν πολυμερής μορφή υψηλού μοριακού βάρους (HMW). Οι βιολογικές της δράσεις ποικίλουν ανάλογα με τη διαφορετική δομή της και τον ιστό που δρα. Έχουν ταυτοποιηθεί τρεις υποδοχείς για την αδιπονεκτίνη AdipoR1, AdipoR2 και η T–cadherin. Η έκφραση AdipoRs επιβεβαιώθηκε σε όλες τις δομές του άξονα υποθαλάμου-υπόφυσης-γονάδες. Αντίθετα η T–cadherin φαίνεται ότι επιδρά μόνο σαν μια δεσμευτική πρωτεΐνη για την αδιπονεκτίνη.
Αδιπονεκτίνη – HPG
Η έκφραση των υποδοχέων της αδιπονεκτίνης έχει επιβεβαιωθεί στον ανθρώπινο υποθάλαμο, όπου εμπλέκεται στη ρύθμιση έκκρισης GnRH, αναστέλλοντάς τη. Η παρουσία της αδιπονεκτίνης και στην υπόφυση, ειδικά στα γοναδοτρόπα κύτταρα, και η επίδρασή της στην απελευθέρωση της LH και FSH, υποδεικνύει το πιθανό ρόλο της αδιπονεκτίνης ως μεταβολικού ρυθμιστή των αναπαραγωγικών λειτουργιών. Τα μέχρι τώρα δεδομένα υποδεικνύουν πιθανό ενδοκρινικό, παρακρινικό και αυτοκρινικό ρόλο τη αδιπονεκτίνης στη ρύθμιση της λειτουργίας των ωοθηκών. Η αδιπονεκτίνη φαίνεται ότι ρυθμίζει τη στεροειδογένεση από τα κοκκιώδη κύτταρα και τα κύτταρα θήκης, αν και τα ευρήματα δεν είναι σταθερά.
Η αδιπονεκτίνη μπορεί να είναι ένας παθοφυσιολογικός σύνδεσμος μεταξύ μεταβολικών διαταραχών (αντίσταση στην ινσουλίνη και παχυσαρκία) και διαταραχών γονιμότητας που απαντώνται σε ασθενείς με PCOS.
Επιπλέον, η αδιπονεκτίνη και οι υποδοχείς της εκφράζονται στο ανθρώπινο ενδομήτριο και έχει παρατηρηθεί μια ισχυρή έκφραση των υποδοχέων της στο ενδομήτριο κατά τη διάρκεια εμφύτευσης του εμβρύου. Μείωση της έκφρασης των AdipoR1 και AdipoR2 παρατηρήθηκε επίσης στο ενδομήτριο γυναικών με επαναλαμβανόμενες αποτυχίες εμφύτευσης σε σύγκριση με γόνιμες γυναίκες, υποδεικνύοντας ένα σημαντικό ρόλο της αδιπονεκτίνης στην ενδομήτρια υποδεκτικότητα και τη πιθανή συμβολή της σε αποτυχίες εμφύτευσης και απώλεια εγκυμοσύνης σε γυναίκες με μεταβολικές παθήσεις όπως η παχυσαρκία και PCOS.
Άλλες αδιποκίνες που σχετίζονται με την αναπαργωγή
Η Chemerin είναι μία προφλεγμονώδης αδιποκίνη που αρχικά παράγεται σαν μία πρωτεΐνη 163 αμινοξέων την pre–pro–chemerin, από την οποία με διάσπαση προκύπτει η αδρανής μορφή pro–chemerin, από την οποία με διαδοχικές πρωτεολυτικές διασπάσεις προκύπτουν διάφορες ισομορφές δραστικής chemerin. Η βιολογική δραστικότητα της chemerin εξαρτάται από το σημείο διάσπασης, το πρωτεολυτικό ένζυμο και το όργανο στόχος. Η chemerin και οι υποδοχείς της βρίσκονται σε όλο το σώμα και τα έως σήμερα ευρήματα δείχνουν ότι διαδραματίζει έναν πολύ-λειτουργικό ρόλο ως ρυθμιστής αρκετών φυσιολογικών διεργασιών, όπως ο έλεγχος της ΑΠ, η αγγειογένεση, η φλεγμονή, η ρύθμιση του ανοσοποητικού και του αναπαραγωγικού συστήματος. Η Chemerin ασκεί τις δράσεις της μέσω σύνδεσης με τρεις διαφορετικούς υποδοχείς: τον CMKLR1 (chemokine like receptor 1), τον GPR1 (G–protein–coupled receptor 1), CCRL2 (chemokine like receptor 2). Στους ανθρώπους, οι συγκεντρώσεις της Chemerin στο πλάσμα σχετίζονται με το σωματικό λίπος και είναι αυξημένες σε ασθενείς με παχυσαρκία και/ή ΣΔ και σε φλεγμονώδεις καταστάσεις. Επιπλέον λειτουργεί χημειοτακτικά στα κύτταρα του ανοσοποιητικού, προκαλεί βλάβη στα αγγεία, μπορεί να παίζει ρόλο στη γένεση των στρωματικών κυττάρων του λίπους, μπορεί να επηρεάζει την αντίσταση στην ινσουλίνη, αυξάνει την οστεοκλαστική δραστηριότητα, αυξάνει την αντίσταση στην ινσουλίνη στο μυϊκό ιστό.
Η Chemerin είναι μια βασική ορμόνη που συνδέει τις αναπαραγωγικές και μεταβολικές λειτουργίες. Μπορεί να παίζει έναν παρακρινό ή/και αυτοκρινό ρυθμιστικό ρόλο στις ωοθήκες. Επηρεάζοντας αρνητικά τη στεροειδογένεση και συμμετέχοντας στη παύση της ανάπτυξης των ωοθυλακίων με άντρο, η Chemerin φαίνεται να παίζει σημαντικό ρόλο στη παθολογική διαδικασία του PCOS. Έχει υποτεθεί ότι παίζει ρόλο στη πλακουντοποίηση και μπορεί να έχει ένα ρόλο στην εμβρυική ανάπτυξη.
Η Resistin είναι ένα προπεπτίδιο 108 αμινοξέων και σχηματίζει συμπλέγματα υψηλού και χαμηλού μοριακού βάρους. Οι δεσμοί δισουλφιδίου και μη-δισουλφιδίου παίζουν επίσης σημαντικό ρόλο στο σχηματισμό μορφών διμερούς, τριμερούς και εξαμερούς κυκλοφορούσας Resistin. Τα λιποκύτταρα δεν είναι η κύρια πηγή της κυκλοφορούσας Resistin στους ανθρώπους. Τα μονοπύρηνα κύτταρα περιφερικού αίματος, τα μακροφάγα κύτταρα και τα κύτταρα μυελού των οστών είναι η κύρια πηγή. Η Resistin επηρεάζει λειτουργικά το μεταβολισμό της γλυκόζης και έχει συσχετιστεί στους ανθρώπους με χρόνιες φλεγμονώδεις και αυτοάνοσες ασθένειες. Αναφορές δείχνουν ότι η Resistin εκφράζεται στον άξονα υποθάλαμος-υπόφυση-γονάδες και ρυθμίζει διάφορες αναπαραγωγικές λειτουργίες. Τα αποτελέσματα σχετικά με τα επίπεδα της Resistin σε ασθενείς με PCOS εξακολουθούν να είναι αμφιλεγόμενα. Φαίνεται να είναι παρούσα στο πλακούντα και μπορεί να συμβάλλει στον έλεγχο της αγγειακής ανάπτυξης του πλακούντα. Η έκφραση της Resistin στο πλακούντα είναι σημαντικά υψηλότερη στο τελευταίο τρίμηνο από ότι στο πρώτο τρίμηνο και μπορεί να εμπλέκεται στην υπερβολική φλεγμονώδη απόκριση της μητέρας που σχετίζεται με τη παθογένεια της προεκλαμψίας.
Η Omentin, που ονομάζεται επίσης και Omentin-1, είναι μια νέα πρωτείνη που παράγεται κυρίως από το σπλαχνικό λίπος στους ανθρώπους. Η έκφραση της Omentin-1 έχει επίσης ανιχνευθεί στους ανθρώπους και σε άλλους ιστούς σε χαμηλά επίπεδα, μεταξύ των οποίων και οι αναπαραγωγικοί ιστοί. Η Omentin-1 αυξάνει τη δράση της ινσουλίνης, σχετίζεται αντιστρόφως με τη παχυσαρκία και αυξάνεται με την απώλεια βάρους. Ευρήματα δείχνουν ότι η Omentin-1 μπορεί να επηρεάζει την έκκριση ορμονών που ρυθμίζουν την ωοθηκική και εμμηνορρυσιακή λειτουργία ή να επηρεάζει τους υποδοχείς αυτών των ορμονών. Τα επίπεδα Omentin-1 πλάσματος είναι υψηλότερα στις γυναίκες από τους άντρες και μειώνονται σε γυναίκες με PCOS σε σύγκριση με γυναίκες χωρίς PCOS και ίδιο ΒΜΙ. Η Omentin-1 έχει συνδεθεί με το μεταβολικό συνδρομο και το PCOS. Η Omentin-1 φαίνεται ότι μπορεί να εμπλέκεται στην ωοθυλακιογένεση και μπορεί να συμβάλει στη παθοφσιολογία του PCOS.
Η Visfatin είναι μια πρωτείνη 491 αμινοξέων που εκφράζεται σε διάφορους ιστούς, αλλά κυρίως στο σπλαχνικό λιπώδη ιστό. Η Visfatin παρουσιάζει μιμητικές δράσεις της ινσουλίνης. Ο υποδοχέας της είναι ακόμη άγνωστος καθώς και η εμπλεκόμενη οδός σηματοδότησης. Στα θηλαστικά η Visfatin ή το NAMPT υπάρχει σε δύο μορφές, την ενδοκυττάρια και την εξωκυττάρια (iNAMPT, eNAMPT). Ενώ η λειτουργία του iNAMPT έχει εδραιωθεί σταθερά ως ένα βιοσυνθετικό ένζυμο NAD και έχει σημαντικό ρόλο στα μιτοχόνδρια, η λειτουργία του eNAMPT είναι αμφιλεγόμενη. Η Visfatin δρα επίσης ως κυτταρικίνη που εμπλέκεται στο μεταβολισμό (παχυσαρκία, διαβήτης τύπου 2) και ανοσολογικές διαταραχές. Έχει βρεθεί ότι τα επίπεδα της Visfatin στον ορό μειώνονται σε γυναίκες με προεκλαμψία και μειώνονται περαιτέρω στη σοβαρή μορφή της νόσου. Παρότι στον άνθρωπο ο ακριβής αναπαραγωγικός ρόλος της Visfatin παραμένει αναμφισβητούμενος, αρκετές μελέτες έδειξαν ότι η visfatin στην ωοθήκη εμφανίζει προ-φλεγμονώδεις ιδιότητες και ανοσολογικές δράσεις, υποδεικνύοντας ένα πιθανό ρόλο στη παθογένεια του PCOS.
Η ανθρώπινη Apelin εντοπίζεται με τη μορφή της preproapelin (77αμινοξέα) που θα διασπαστεί από ενδοπεπτιδάσες και θα προκύψει η proapelin (55 αμινοξέα) και στη συνέχεια σε άλλες ενεργείς ισομορφές (36,17,13 και Pyr-13 αμινοξέα). Η Apelin εκφράζεται ευρέως σε διάφορους τύπους ιστών και όργανα (κεντρικό νευρικό σύστημα, υποθάλαμος, λιπώδης ιστός, σκελετικός μυς, πεπτικό σύστημα και ωοθήκες). Σηματοδοτεί μέσω του υποδοχέα εξαρτώμενου από G πρωτεΐνη (APLNR). Βελτιώνει την αντίσταση στη γλυκόζη και την ευαισθησία στην ινσουλίνη, συμβάλλει στην ομοιόσταση των βιολογικών υγρών, μπορεί να επηρεάζει τη μυϊκή μάζα, αυξάνει τη πρόσληψη γλυκόζης από τα κύτταρα του λιπώδους και του μυϊκού ιστού, αυξάνει τη θερμογένεση από το λιπώδη ιστό και την αγγειογένεση, αυξάνει τη κατανάλωση ενέργειας, τη λεμφαγγειογένεση, τη βιογένεση μιτοχονδρίων στο μυϊκό ιστό και την οξείδωση των λιπαρών οξέων, συμβάλλει στην ελάττωση του σωματικού βάρους, της ΑΠ, τέλος μπορεί να ελαττώσει τη φλεγμονή και την ηπατική στεάτωση. Τα έως τώρα ευρήματα υποδεικνύουν ένα ρόλο της Apelin στην ορμονική ρύθμιση της ωοθηκικής λειτουργίας και υποστηρίζουν τη πιθανή εμπλοκή της Apelin στις διαταραχές του άξονα υποθαλάμου-υπόφυσης-ωοθηκών και στην ωοθηλακιορρηκτική δυσλειτουργία που συνδέεται με το PCOS. Η Apelin εκφράζεται επιπλέον στον ανθρώπινο πλακούντα. Το σύστημα Apelin/APJ μπορεί να έχει ρόλο στη παθογένεια της προεκλαμψίας.
Συμπεράσματα
Ο λιπώδης ιστός και το κύριο συστατικό του, τα λιποκύτταρα, είναι απαραίτητα για την επιβίωση. Προστατεύουν το σώμα από από το τραύμα, παρέχουν τη κύρια πηγή αποθηκευμένης ενέργειας και επηρεάζουν μια πληθώρα φυσιολογικών λειτουργιών, συμπεριλαμβανομένης της αναπαραγωγής, μέσω μιας σειράς εκκρινόμενων προϊόντων, συλλογικά γνωστών ως αδιποκίνες. Είναι πλέον σαφές ότι ο λιπώδης ιστός επικοινωνεί με τον εγκέφαλο, τις γονάδες και τη μήτρα για να ρυθμίζει τις αναπαραγωγικές λειτουργίες μέσω αυτών των αδιποκινών και κατά συνέπεια οι αδιποκίνες συμμετέχουν στη εξήγηση ορισμένων αναπαραγωγικών διαταραχών. Αυτές οι αδιποκίνες έχουν ωφέλιμες ή ασκούν αρνητικές επιδράσεις στη γονιμότητα του ανθρώπου; Οι περισσότερες μελέτες έχουν γίνει σε in vitro κύτταρα των ωοθηκών και οι in vivo μελέτες είναι περιορισμένες, οπότε είναι δύσκολο να δοθεί απάντηση για ολόκληρο τον οργανισμό. Μερικές φορές τα δεδομένα in vitro είναι αντιφατικά, γεγονός που μπορεί να εξηγηθεί από διαφορές ανάλογα με το είδος, αλλά και από τη χρήση διαφορετικών συγκεντρώσεων των αδιποκινών ή/και διαφορετικού πειραματικού σχεδιασμού. Είναι ενδιαφέρον ότι η έκφραση των αδιποκινών στο πλάσμα ή και στους ιστούς μπορεί να σχετίζεται με διάφορες γυναικείες αναπαραγωγικές διαταραχές συμπεριλαμβανομένου του συνδρόμου PCOS, του διαβήτη κύησης, της προεκλαμψίας, της ενδομήτριας καθυστέρησης της ανάπτυξης του εμβρύου. Απαιτούνται πρόσθετες μελέτες για τη καλύτερη κατανόηση του ρόλου και του μοριακού μηχανισμού των αδιποκινών στον έλεγχο της γονιμότητας προκειμένου να χρησιμοποιηθούν ενδεχομένως ως προγνωστικοί δείκτες ή/και θεραπευτικοί στόχοι σε διάφορες αναπαραγωγικές διαταραχές.
Βιβλιογραφία
- Biochemistry of adipose tissue: an endocrine organ
Arch Med Sci 2013; 9, 2: 191-200 DOI: 10.5114/aoms.2013.33181 Copyright © 2013 Termedia & Banach
- Role of leptin in female reproduction Clin Chem Lab Med 2015; 53(1): 15–28
Antonio Pérez-Pérez, Flora Sánchez-Jiménez, Julieta Maymó, José L. Dueñas, Cecilia Varone and Víctor Sánchez-Margalet*
DOI 10.1515/cclm-2014-0387 Received April 8, 2014; accepted June 16, 2014; previously published online July 11, 2014
- The role of visfatin in the pathogenesis of gestational diabetes (GDM) Sandra Radzicka, Marek Pietryga, Rafał Iciek, Jacek Brązert Department of Obstetrics and Women Diseases, University of Medical Science, Poznań, Poland
Ginekologia Polska 2018, vol. 89, no. 9, 518–521 Copyright © 2018 Via Medica ISSN 0017–0011 DOI: 10.5603/GP.a2018.0088
- Adipocytokines: mediators linking adipose tissue, inflammation and immunity
DOI: 10.1038/nri1937
- Beyond adiponectin and leptin: adipose tissue-derived mediators of inter-organ communication
Jan-Bernd Funcke and Philipp E. Scherer1 Touchstone Diabetes Center, University of Texas Southwestern Medical Center, Dallas, TX ORCID IDs: 0000-0002-2596-3167 (J-B.F.); 0000-0003-0680-3392 (P.E.S.)
TrueMed-ForLivingMore
Κοινοποιήστε
ΔΙΑΒΑΣΤΕ ΕΠΙΣΗΣ
Βρείτε μας στο Facebook
Και στο Instagram
Επικοινωνία
Η ομάδα μας
Διαφημιστείτε στη truemed.gr
Όροι χρήσης
Προσωπικά δεδομένα
Copyright©Truemed
Για περισσότερη ζωή
Designed – Developed by Premiumweb.gr

© 2019 TrueMed Media. All rights reserved. Our website services, content, and products are for informational purposes only. TrueMed Media does not provide medical advice, diagnosis, or treatment.
Αρθρογράφος
Γεννηθείσα 16/06/1999 στο Μαρούσι Αττικής με τόπο καταγωγής τη Χαλκίδα, Ευβοίας. Από μικρή απολάμβανε την επαφή με τη φύση, τα ντοκιμαντερ και τη ζωγραφική.
Η αγάπη για την ιατρική και το ανθρώπινο σώμα ξεκίνησε από πολύ νωρίς να εμφανίζεται, επηρεασμένη από γονεϊκά πρότυπα. Στο γυμνάσιο και το λύκειο ήρθε σε επαφή με το αντικείμενο παρακολουθώντας Χειρουργικές επεμβάσεις.
Ως φοιτήτρια Ιατρικής στο ΔΠΘ σήμερα προσπαθεί να κατανοήσει σε βάθος τη πολυπλοκότητα αυτής Επιστήμης αυτής, έχοντας θάρρος, όρεξη και αγάπη γι’ αυτή.
Βασική εκπαίδευση
2007-2013:7ΟΔΗΜΟΤΙΚΟ ΧΑΛΚΙΔΑΣ
2013-2015:1ΟΓΥΜΑΝΣΙΟ ΧΑΛΚΙΔΑΣ
2015-2017: 1οΓΕΛ ΧΑΛΚΙΔΑΣ
ΠΑΝΕΠΙΣΤΗΜΙΑΚΕΣ ΣΠΟΥΔΕΣ
ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΔΗΜΟΚΡΙΤΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΡΑΚΗΣ
ΕΤΟΣ ΕΙΣΑΓΩΓΗΣ: 2017
ΞΈΝΕΣ ΓΛΩΣΣΕΣ
Αγγλικά : FCE (Cambridge English: First), επιπέδου B2 (University of Cambridge)
Γερμανικά: Goethe-Zertifikat B2
Συμμετοχή και Παρακολούθηση
- Ομιλία «Η Ανοσοθεραπεία στο Καρκίνο της Ουροδόχου Κύστεως και Νεφρών» στο 10o ΣΥΝΕΔΡΙΟ Ε.Δ.Ε.Μ.Σ.Ε.Θ., 7-8 Μαΐου 2021
- Συμμετοχή και Παρακολούθηση στο 27ο Επιστημονικό Συνέδριο Φοιτητών Ιατρικής Ελλάδας & 15ο Διεθνές Forum Φοιτητών Ιατρικής και Νέων Ιατρών
Ομιλία «Πρόληψη Σεξουαλικής Κακοποίησης Ανηλίκων» Τράπεζα Ιατροδικαστικής
- Συμμετοχή στο Webinar Παχυσαρκία: Από την Αιτιοπαθογένεια στη Θεραπεία 24/04/ 2021
- Συμμετοχή στην Ημερίδα Απεικόνιση Παιδιατρικού Θώρακα: Από την πλευρά του Παιδιάτρου και του Ακτινολόγου 3/04/ 2021
- Συμμετοχή στη διοργάνωση του Webinar της ΕΕΦΙΕ του παραρτήματος Αλεξανδρούπολης "Επείγοντα περιστατικά με Έμφαση στο αγροτικό"
- Παρακολούθηση:Η Παθολογία της Κύησης σε 40 Ερωτήσεις (WEB CONGRESS) // 5-6-7 /03/ 2021
- Συμμετοχή στο 29ο Πανελλήνιο Πνευμονολογικό Συνέδριο
- Παρακολούθηση KIDS SAVE LIVES - Τα Παιδιά Σώζουν Ζωές
- Ομιλία «ΙΦΝΕ και COVID-19» στο 1o Πανελλήνιο Διαδικτυακό Συνέδριο Ιατρικής Βιοπαθολογίας, το οποίο διοργανώθηκε από την Πανελλήνια Ένωση Ιατρικής Βιοπαθολογίας και την Ελληνική Εταιρεία Ιατρικής Βιοπαθολογίας/ Εργαστηριακής Ιατρικής διαδικτυακά στις 11-13 Δεκεμβρίου 2020.
- Παρακολούθηση στο 25ου Επιστημονικό Συνέδριο Φοιτητών Ιατρικής Ελλάδας & 15ο Διεθνές Forum Φοιτητών Ιατρικής και Νέων Ιατρών
Αριθμός άρθρων που έχει γράψει στην Truemed: 2