For Living More⚕️
🚑 Εφημερεύοντα φαρμακεία / Τηλέφωνα Α’ Ανάγκης 🚑
Βρες τις χαμηλότερες τιμές φαρμάκων 💊
Parkinson: απο την αιτιοπαθογένεια στη θεραπεία
![]() 29-7-2020
29-7-2020
![]() Ιωάννης Κουκουλίθρας
Ιωάννης Κουκουλίθρας
![]() Αλεξάνδρα Σταμούλη
Αλεξάνδρα Σταμούλη
![]() Μηνάς Πλεξουσάκης
Μηνάς Πλεξουσάκης
![]() Σπυρίδων Κολοκώτσιος
Σπυρίδων Κολοκώτσιος
Ο παρκινσονισμός είναι ένας ευρύς όρος που μελετά το σύνολο των σημείων και των συμπτωμάτων που χαρακτηρίζουν τη νόσο του Parkinson.
Τον πιο συχνό τύπο παρκινσονισμού, περίπου το 80-85% των περιπτώσεων ,αποτελεί ο ιδιοπαθής/πρωτοπαθής παρκινσονισμός ή νόσος του Parkinson. Ο τύπος αυτός αποκρίνεται καλά στα φάρμακα τα οποία έχουν ως σκοπό την αύξηση ή υποκατάσταση της ντοπαμίνης.
Το υπόλοιπο 10-15% των περιπτώσεων αποτελεί ο δευτεροπαθής/άτυπος παρκινσονισμός , ο οποίος είναι απόρροια άλλων παθήσεων και πιθανώς σχετίζεται με εγκεφαλίτιδα, αλκοολισμό, έκθεση σε ορισμένες τοξικές ουσίες, κρανιοεγκεφαλικές κακώσεις, αγγειακά εγκεφαλικά επεισόδια (Vascular parkinsonism) και χρήση ψυχοτρόπων φαρμάκων ( Drug-induced Parkinsonism). Είναι δύσκολο να γίνει η διαφοροποίησή τους από τον πρωτοπαθή παρκινσονισμό.
Τα σύνδρομα Parkinson’s Plus αποτελούν ένα σύνολο παθήσεων-διαταραχών που εκδηλώνονται σαν την νόσο του Parkinson. Ασθενείς με δευτεροπαθή παρκινσονισμό δεν ανταποκρίνονται καλά σε ντοπαμινεργικές φαρμακευτικές αγωγές, όπως για παράδειγμα η Levodopa και είναι πιο δύσκολη η αντιμετώπιση από αυτούς με νόσο του Parkinson. Τέτοια σύνδρομα αποτελούν:
· η ατροφία πολλαπλών συστημάτων (Multiple System Atrophy ή MSA)
· η προοδευτική υπερπυρηνική παράλυση (Progressive Supranuclear Palsy ή PSP)
· το κορτικοβασικό σύνδρομο (Corticobasal Syndrome ή CBS)
Στα σύνδρομα Parkinson’s Plus εκτός από τα συμπτώματα που οφείλονται στην εκφύλιση της μέλαινας ουσίας, συνυπάρχουν και άλλα νευρολογικά σημεία που σχετίζονται με την δυσλειτουργία της παρεγκεφαλίδας και του αυτονόμου νευρικού συστήματος.
Νόσος Parkinson
Η νόσος Parkinson όπως περιγράφηκε για πρώτη φορά από τον James Parkinson το 1817 είναι η δεύτερη πιο συχνή νευροεκφυλιστική νόσος (μετά τη νόσο Alzheimer) η οποία χαρακτηρίζεται από βραδυκινησία, δυσκαμψία , τρόμο ηρεμίας , συρόμενο βάδισμα, παγωμένο προσωπείο. Προσβάλλει περισσότερο από 1 εκατομμύριο άτομα στην Ευρώπη και το οικονομικό αντίκτυπο της νόσου είναι τεράστιο. Εκτιμάται περίπου σε 13,3 δις στην Ευρώπη το έτος. Το 2003 στο Ηνωμένο βασίλειο το ετήσιο κόστος φροντίδας για κάθε ασθενή με νόσο Πάρκινσον ήταν 9.975 Ευρώ. Η έναρξη των συμπτωμάτων εκτιμάται τα 40-70 έτη με κορύφωση τα 60 έτη. Η πορεία της νόσου κυμαίνεται από 10 έως 25 έτη.
Πρόκειται για μία διαταραχή του εξωπυραμιδικού συστήματος και συγκεκριμένα του κυκλώματος των βασικών γαγγλίων το οποίο ρυθμίζεται από την παρουσία ντοπαμίνης. Παρατηρείται εκφύλιση των ντοπαμινεργικών νευρώνων της συμπαγούς μοίρας της μέλαινας ουσίας στο μέσο εγκέφαλο με ταυτόχρονη προσβολή της μελαινο-ραβδωτής οδού. Το κύκλωμα των βασικών γαγγλίων το οποίο αποτελείται ανατομικά από τον κερκοφόρο π. , το κέλυφος , την ωχρά σφαίρα , προτείχισμα , αμυγδαλοειδή π. συμμετέχει στον έλεγχο των κινήσεων, των μεμαθημένων κινήσεων και της στάσης. Αποτελείται από GABA εργικούς νευρώνες(ανασταλτικούς) , με εξαίρεση των υποθαλάμιο πυρήνα ο οποίος είναι Glutaminergic (διεγερτικός) Το κύκλωμα αυτό διαχωρίζεται σε άμεσο διεγερτικό και έμμεσο ανασταλτικό. Το σχήμα 1 παρουσιάζει τις συνδέσεις του κυκλώματος αυτού σε φυσιολογικές συνθήκες και στη νόσο Parkinson. Στην νόσο Parkinson, λόγω της ντοπαμινεργικής εκφύλισης υπολειτουργεί το άμεσο διεγερτικό κύκλωμα και υπερλειτουργεί το έμμεσο ανασταλτικό , με αποτέλεσμα να μην στέλνονται ώσεις στους πυρήνες του θαλάμου(οπίσθιοι κοιλιακοί πλάγιοι) , οι οποίοι με την σειρά τους δεν στέλνουν ευοδωτικά ερεθίσματα στον κινητικό φλοιό του εγκεφάλου (π.4, π.6 Brodmann). Το αποτέλεσμα είναι κυρίως βραδυκινησία και δυσκαμψία. Να σημειωθεί ότι οι D1 υποδοχείς του ραβδωτού σώματος στο άμεσο κύκλωμα έχουν διεγερτικό ρόλο ,ενώ οι D2 υποδοχείς στο έμμεσο κύκλωμα έχουν ανασταλτικό ρόλο.

Παρά τις εντατικές έρευνες που έχουν γίνει και συνεχίζουν να γίνονται ακόμα, η ακριβής αιτιολογία της νόσου Πάρκινσον δεν είναι ακόμη γνωστή. Ποικίλοι μηχανισμοί έχουν αναφερθεί στη διεθνή βιβλιογραφία που προκαλούν εκφύλιση των ντοπαμινεργικών νευρώνων, ωστόσο αυτή της μιτοφαγίας κερδίζει όλο και περισσότερο έδαφος τα τελευταία χρόνια. Πιθανολογείται ότι υπάρχει μία πολυσύνθετη αλληλεπίδραση μεταξύ γενετικών και περιβαλλοντικών παραγόντων. Οι παράγοντες κινδύνου περιλαμβάνουν: θετικό οικογενειακό ιστορικό , άρρεν φύλο, κρανιοεγκεφαλική κάκωση, έκθεση σε εντομοκτόνα, κατανάλωση νερού από πηγές και την διαμονή στην ύπαιθρο. Τα ακριβή αίτια αναλύονται παρακάτω.
MPTP (1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine).
Το 1983 στην Καλιφόρνια των Η.Π.Α παρουσιάστηκε ραγδαία αύξηση των ατόμων που παρουσίαζαν συμπτώματα Παρκινσονισμού. Έρευνες της εποχής έδειξαν ότι ένα από τα συστατικά των ναρκωτικών ουσιών που χρησιμοποιούνταν ήταν το MPTP. Το MPTP μεταβολίζεται σε νευροτοξίνη MPP+ , η οποία είναι ένας εκλεκτικός αναστολέας του μιτοχονδριακού συμπλόκου 1 της αναπνευστικής αλυσίδας στους νευρώνες της μέλαινας ουσίας. Αυτό οδηγεί στην δημιουργία ελεύθερων ριζών, μεταλλάξεων στο μιτοχονδριακό DNA και τελικά ντοπαμινεργική εκφύλιση.
Μελέτες έχουν δείξει ότι τα επίπεδα του ελεύθερου σιδήρου είναι ταυτόχρονα αυξημένα.
Γενετικά
Παρόλο που το Πάρκινσον θεωρείται μία ιδιοπαθής νόσος μόνο το 15% των ασθενών παρουσιάζει οικογενειακό ιστορικό. 23 γονίδια έχουν συνδεθεί με τη νόσο Πάρκινσον αν και τα τελευταία χρόνια αυξάνονται.
Ο πίνακας 1 παρουσιάζει κάποια από τα γονίδια που συμμετέχουν στη νόσο Πάρκινσον.
|
Γενετική Θέση |
Γονίδιο |
Πρωτεΐνη |
Λειτουργία |
Κληρονομικότητα |
|
PARK1 |
SNCA |
α-συνουκλεΐνη |
Κυκλοφορία κυστιδίων Ντοπαμίνης |
ΑΕ |
|
PARK2 |
PRKN |
Παρκίνη |
Λιγάση Ε3 ουμπικιτίνης |
ΑΥ |
|
PARK4 |
SNCA |
α-συνουκλεΐνη |
Κυκλοφορία κυστιδίων Ντοπαμίνης |
ΑΕ |
|
PARK5 |
UCH-L1 |
UCH-L1 |
Υδροξυλάση L1 -COOH της Ουμπικιτίνης |
ΑΕ |
|
PARK6 |
PINK |
PINK 1 |
Μιτοχονδριακή κινάση |
ΑΥ |
Πίνακας 1: Παρουσιάζει τις πιο συνηθισμένες γονιδιακές μεταλλάξεις , τις επιπτώσεις τους και την κληρονομικότητα. Από Harrison, Νευρολογία στην Κλινική Ιατρική, εκδόσεις Παρισιάνος
Από τις συνηθισμένες μεταλλάξεις είναι του γονιδίου PARK1 το οποίο κωδικοποιεί την α -συνουκλεΐνη , μία πρωτεΐνη η οποία συμμετέχει στην ανακύκλωση των κυστιδίων που περιέχουν το νευροδιαβιβαστή ντοπαμίνη στους ντοπαμινεργικούς νευρώνες της μέλαινας ουσίας. Η α- συνουκλεΐνη είναι μία μη αναδιπλωμένη πρωτεΐνη. Μετάλλαξή της οδηγoούν σε λανθασμένη αναδίπλωση αυτής της πρωτείνης , δημιουργία β- πτυχωτής επιφάνειας , συσσωματωμάτων α – συνουκλεΐνη και τελικά φλεγμονή στην περιοχή με ντοπαμινεργική εκφύλιση. Στις ιστολογικές εξετάσεις παρουσιάζονται τα σωμάτια Lewy τα οποία είναι έγκλειστα α-συνουκλεΐνης χαρακτηριστικό παθολογοανατομικό στοιχείο της νόσου Πάρκινσον. Σωμάτια Lewy μπορεί να παρατηρηθούν αρχικά στους οσφρητικούς βολβούς αλλά και σε περιοχές όπως του μεταιχμιακού συστήματος, εγκεφαλικών συζυγιών , μετωπιαίου λοβού, συμπαγούς μοίρας μέλαινας ουσίας κτλ. Το σχήμα 2 δείχνει σωμάτια Lewy σε νευρικά κύτταρα της μέλαινας ουσίας.

Ουβικιτινίωση-Πρωτεάσωμα
Για την φυσιολογική λειτουργία των πρωτεϊνών είναι απαραίτητο να συντίθενται και να αναδιπλώνονται σωστά στο χώρο , μέχρι να πάρουν την τριτοταγή – τεταρτοταγή δομή τους. Πρωτεΐνες στις οποίες δεν έχει γίνει σωστή αναδίπλωση τους και οι μοριακοί συνοδοί δεν κατάφεραν να τις επιδιορθώσουν θα πρέπει να αποικοδομηθούν. Αυτό γίνεται μέσω ενός πολύπλοκου μηχανισμού στον οποίο συμμετέχει η ουβικιτινίωση- πρωτεάσωμα. Μεταλλάξεις των γονιδίων PARK5 και PARK2 τα οποία κωδικοποιούν πρωτεΐνες οι οποίες συμμετέχουν στον μηχανισμό του συστήματος ουβικιτινίωσης -πρωτεασώματος οδηγούν στη νόσο Πάρκινσον. Πιο συγκεκριμένα, η δυσλειτουργία της παρκίνης μπορεί από την μια να οδηγεί σε συνεχή και παθολογική ουβικιτινίωση πρωτεϊνών και τελικά ντοπαμινεργική εκφύλιση , και από την άλλη να μην μπορεί να κάνει ουβικιτινίωση των μεταλλαγμένων υποστρωμάτων π.χ α – συνουκλεΐνης , γεγονός που οδηγεί στην συσσώρευση του υποστρώματος (α -συνουκλεΐνης)
Μιτοχονδριακή δυσλειτουργία
Αποτελεί την πιο συχνή αιτία στην ιδιοπαθή και οικογενή νόσο Πάρκινσον. Μελέτες των μιτοχονδρίων των νευρώνων της συμπαγούς μοίρας της μέλαινας ουσίας σε ασθενείς με νόσο Πάρκινσον έχουν δείξει ότι υπάρχει έλλειψη του μιτοχονδριακού συμπλόκου 1 που συμμετέχει στην μεταφορά των ηλεκτρονίων στην αναπνευστική αλυσίδα. Αυτό οδηγεί στην δημιουργία ROS τα οποία είναι πολύ δραστικά μόρια και δημιουργούν μεταλλάξεις. Επιπλέον, μεταλλάξεις των γονιδίων PINK1 και παρκίνης τα οποία είναι απαραίτητα για την απομάκρυνση των δυσλειτουργικών μιτοχονδρίων οδηγούν στην μη φυσιολογική πορεία της διαδικασίας της μιτοφαγίας.
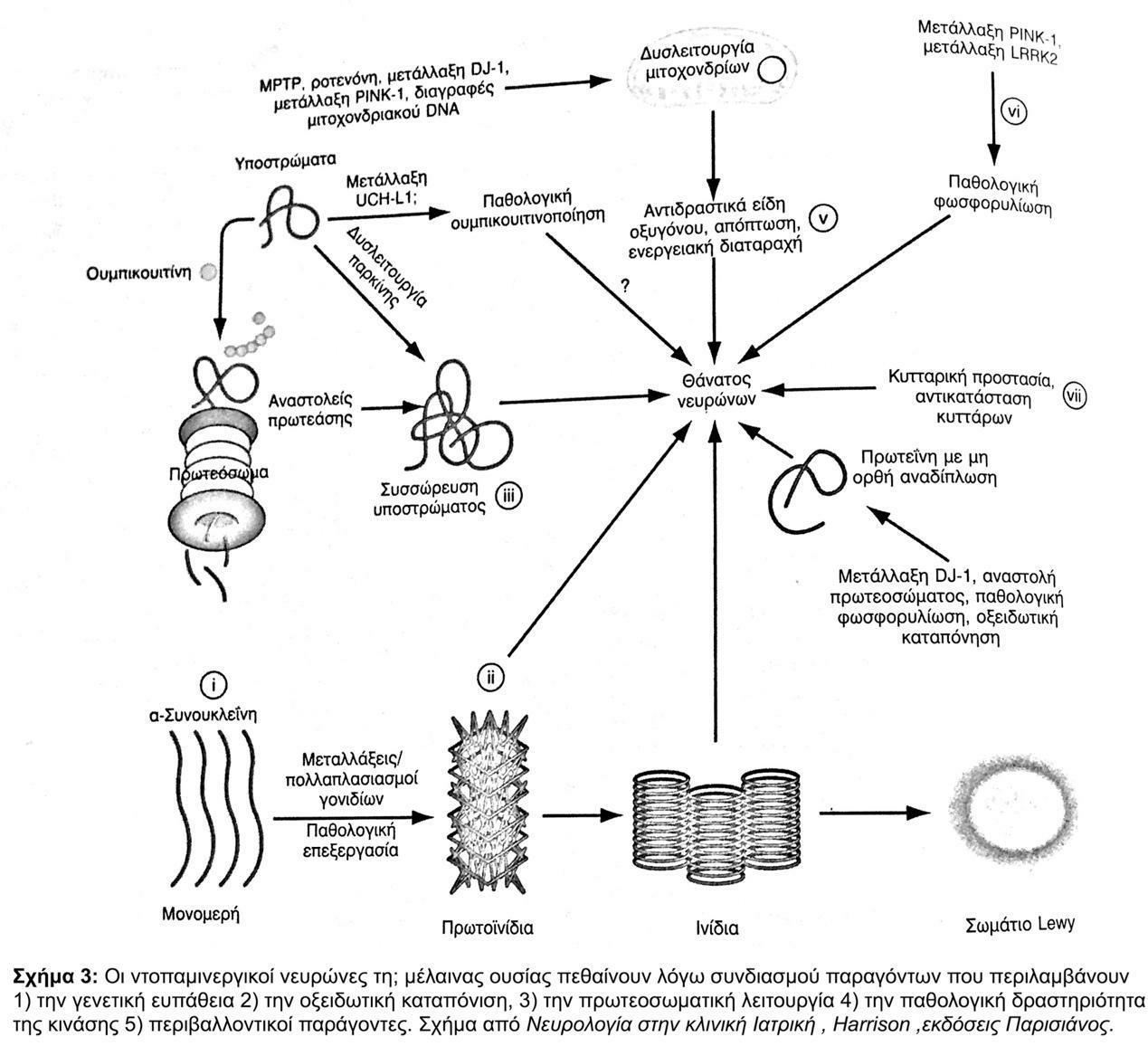
Το σχήμα 3 συνοψίζει τις αιτίες ντοπαμινεργικής εκφύλισης.
Αυτοανοσία και Parkinson
Νεότερες μελέτες έχουν δείξει ότι υπάρχει αυξημένη συσχέτιση της νόσου Πάρκινσον με αυτοάνοσες καταστάσεις. Μια μεγάλη επιδημιολογική μελέτη η οποία διεξήχθη στη Σουηδία και στην οποία συμμετείχαν περισσότεροι από 310.000 ασθενείς με αυτοάνοσα νοσήματα (π.χ σκλήρυνση κατά πλάκας, Hashimoto, νόσο Graves, πλάγια μυατροφική σκλήρυνση (ALS) κ.ά.) έδειξε ότι αυτοί οι ασθενείς είχαν 33% πιθανότητα να εμφανίσουν και νόσο Parkinson (Li, X., Sundquist et.al.) Ειδικότερα, ασθενείς που έπασχαν από σύνδρομο Sjögren είχαν ακόμη μεγαλύτερη πιθανότητα. Η συσχέτιση της νόσου Parkinson με αυτοάνοσες ασθένειες θα μπορούσε να εξηγηθεί εν μέρει από γενετικές παρεκκλίσεις που είναι κοινές σε αυτές τις καταστάσεις και που επηρεάζουν την ανοσολογική λειτουργία. Λοιμώξεις από την κοινή γρίπη και τον ιό του έρπητα φαίνεται να συμβάλλουν στην νόσο Parkinson. Αυτό φαίνεται να συμβαίνει, διότι κάποια ιϊκή πρωτεΐνη έχει πολύ μεγάλη ομοιότητα με την α- συνουκλεΐνη και έτσι ενεργοποιείται το ανοσοποιητικό σύστημα. Στην αρχή παρατηρείται ενεργοποίηση των μικρογλοιακών κυττάρων τα οποία λειτουργούν ως αντιγονοπαρουσιαστικά στο ΚΝΣ. Στη συνέχεια, εκκρίνουν κυτταροκίνες όπως IL-1β , ΤNFa κτλ. οι οποίες πυροδοτούν να εισέλθουν τα Τ-Λεμφοκύτταρα . Έτσι , δημιουργείται μία φλεγμονή στην περιοχή με τελικό αποτέλεσμα την καταστροφή των ντοπαμινεργικών νευρώνων.
Κάπνισμα
Έχουν γίνει εκτενείς μελέτες σχετικά με την επίδραση του καπνίσματος στην νόσο του Parkinson. Οι περισσότερες καταλήγουν στο συμπέρασμα ότι το κάπνισμα μειώνει την πιθανότητα εμφάνισης νόσου Πάρκινσον . Αυτό συμβαίνει , επειδή ενεργοποιούνται οι νικοτινικοί υποδοχείς των ντοπαμινεργικών νευρώνων και εκκρίνεται ντοπαμίνη. Επιπλέον, η έκκριση ντοπαμίνης συμμετέχει στο μηχανισμό επιβράβευσης(επικλινής πυρήνας). Μελέτες υποστηρίζουν ότι τα άτομα που πάσχουν από Πάρκινσον μπορούν πιο εύκολα να κόψουν το κάπνισμα, καθώς δεν έχουμε έκκριση ντοπαμίνης (δεν έχουμε ανταπόκριση στην παρουσία νικοτίνης), συνεπώς ο μηχανισμός επιβράβευσης μέσω του μεσο-μεταιχμιακού-ντοπαμινεργικού συστήματος δεν λειτουργεί φυσιολογικά.
Καφεΐνη
Η καφεΐνη φαίνεται ότι συμμετέχει και αυτή στην πρόληψη της νόσου Πάρκινσον. Η καφεΐνη είναι ένας α2 αδρενεργικός ανταγωνιστής ,με αποτέλεσμα να εμποδίζεται η επαναπρόσληψη κατεχολαμινών όπως νορεπινεφρίνη, επινεφρίνη, ντοπαμίνη. Ωστόσο, χρειάζονται ακόμη περισσότερες μελέτες για την επιβεβαίωση της αποτελεσματικότητάς της. Ο συνδυασμός χορήγησης οιστρογόνων και κατανάλωσης καφεΐνης στις μετεμμηνοπαυσιακές γυναίκες μειώνει ακόμη περισσότερο την πιθανότητα , καθώς τα οιστρογόνα εμποδίζουν τον μεταβολισμό της καφεΐνης.
Συμπτώματα
Σύμφωνα με νέες μελέτες πριν την εμφάνιση των κινητικών συμπτωμάτων παρατηρείται μια παροδική διαταραχή της όσφρησης και διαταραχή του σταδίου REM κατά την διάρκεια του ύπνου. Τα συμπτώματα αυτά δεν παραπέμπουν σε υποψία έναρξης της νόσου. Η εγκατάσταση της νόσου Parkinson είναι βραδεία και προοδευτική με κύριο σύμπτωμα τον τρόμο ηρεμίας ο οποίος εμφανίζεται σε 70% των ασθενών. Στα βασικά συμπτώματα περιλαμβάνονται η δυσκαμψία , η βραδυκινησία, η κόπωση και η διαταραχή ισορροπίας. Καθώς το Parkinson αποτελεί μια νευροεξελικτική νόσο επιπλέον συμπτώματα που μπορούν να εμφανιστούν είναι η δυσκαταποσία , το πάγωμα βάδισης και η διαταραχή ομιλίας. Όπως και στις περισσότερες νευρολογικές διαταραχές το άτομο μπορεί να εμφανίσει συμπτώματα από το αυτόνομο νευρικό σύστημα ( σιελόρροια, διαταραχές ούρησης, ορθοστατική υπόταση και δυσκοιλιότητα). Τέλος ψυχολογικές διαταραχές όπως άγχος και κατάθλιψη παρουσιάζονται στην πλειοψηφία των ασθενών.
Ο τρόμος ηρεμίας περιλαμβάνει μια συνεχή κίνηση υπτιασμού – πρηνισμού η οποία προσομοιάζει την κίνηση μέτρησης κερμάτων. Η εγκατάσταση ξεκινάει στο ένα χέρι με συχνότερο να είναι το αριστερό και κατα την διάρκεια εξέλιξης της νόσου προσβάλλεται και το άλλο. Χαρακτηριστικό του τρόμου ηρεμίας είναι ότι εξαφανίζεται με την εκούσια κίνηση και κατα την διάρκεια του ύπνου.
Λόγω της εξωπυραμιδικής υπερτονίας παρατηρείται δυσκαμψία, η οποία εκδηλώνεται ως αντίσταση στην παθητική κίνηση ως αποτέλεσμα να εμφανίζονται βραχύνσεις, με την πιο επιρρεπή μυϊκή ομάδα να είναι οι καμπτήρες του γόνατος.
Ως βραδυκινησία ορίζεται η καθυστερημένη έναρξη και η μειωμένη ταχύτητα εκτέλεσης των κινήσεων, ειδικότερα των αυτοματοποιημένων όπως η βάδιση.
Διαταραχές της ισορροπίας εκδηλώνονται με την πρόοδο της νόσου λόγω μειωμένης ανταπόκρισης των αντανακλαστικών της στάσης με αποτέλεσμα οι ασθενείς να παρουσιάζουν αυξημένη τάση προς πτώση. Επιπλέον, έχει παρατηρηθεί ότι ύστερα από την πρώτη πτώση η πιθανότητα για μεταγενέστερες αυξάνεται.
Το Πάγωμα βάδισης αποτελεί σύμπτωμα της φυσικής εξέλιξης της νόσου και εκδηλώνεται ως επεισόδιο ακινησίας κυρίως όταν ο ασθενής επιχειρεί να στρίψει τον κορμό του ή να περάσει μέσα από έναν στενό χώρο όπως μια πόρτα. Για την αντιμετώπιση του παγώματος συνιστώνται ακουστικές υποδείξεις.
Διάγνωση και Κλινική εξέταση
Η διάγνωση της νόσου βασίζεται κυρίως στην ύπαρξη 2 ή περισσότερων βασικών συμπτωμάτων (δυσκαμψία, βραδυκινησία, τρόμος ηρεμίας, διαταραχή ισορροπίας), στον αποκλεισμό των συνδρόμων Parkinson Plus και στην ανταπόκριση στην λεβοντόπα.
Στα κλινικά ευρήματα παρατηρείται ανέκφραστο πρόσωπο, στάση πρόσθιας κλίσης κορμού, κάμψη άνω άκρων στους αγκώνες και στους καρπούς, ελαφριά κάμψη των ισχίων και των γονάτων, μικρά και μπερδεμένα βήματα, επιταχυνόμενη βάδιση, μικρογραφία, μονότονη ομιλία και απουσία αιώρησης άνω άκρων κατά την βάδιση.

Προδιαθεσικοί παράγοντες
|
Αυξημένη χοληστερόλη |
Αυξημένο BMI |
Ιογενείς λοιμώξεις |
|
Έκθεση σε περιβαλλοντικές τοξίνες |
Φλεγμονή που σχετίζεται με ενεργοποίηση μικρογλοικών κυττάρων |
Διαταραχή μηχανισμών απόπτωσης |
|
κρανιοεγκεφαλικές κακώσεις |
χρήση ναρκωτικών ουσιών |
Αλκοολισμός |
|
Υψηλή θερμιδική πρόσληψη |
Μιτοχονδριακή δυσλειτουργία |
Όγκος στα βασικά γάγγλια και στον μετωπιαίο λοβό |
Αντιμετώπιση
Στόχος της θεραπείας στη νόσο Πάρκινσον είναι η διατήρηση της λειτουργικότητας και της ποιότητας ζωής του ασθενούς. Η συμπτωματική θεραπεία είναι αρκετά αποτελεσματική στην αντιμετώπιση του τρόμου ηρεμίας, βραδυκινησίας , δυσκαμψίας. Τα νοητικά συμπτώματα και οι ψυχικές διαταραχές που μπορεί να ακολουθούν δεν μπορούν να αντιμετωπιστούν με την φαρμακευτική αγωγή για την αντιμετώπιση του Πάρκινσον. Πολλές διαφορετικές απόψεις υπάρχουν για την χρονική στιγμή που πρέπει να ξεκινήσει η θεραπεία. Πολλοί πιστεύουν ότι η θεραπεία πρέπει να καθυστερήσει όσο δυνατόν περισσότερο , καθώς τα φάρμακα δεν μπορούν να φέρουν κανένα αποτέλεσμα μετά από κάποιο διάστημα και μπορεί να επιβαρύνουν την κατάσταση ακόμη περισσότερο. Ωστόσο, μοντέρνες απόψεις τονίζουν ότι η θεραπεία θα πρέπει να ξεκινήσει το συντομότερο δυνατόν για την διατήρηση επαρκούς επιπέδου νοητικής και σωματικής δραστηριότητας. Η φαρμακευτική αγωγή σε συνδυασμό με ένα κατάλληλο και εξατομικευμένο πρόγραμμα φυσικοθεραπείας αποτελούν θεραπεία εκλογής για τη νόσο Πάρκινσον.
Υπάρχουν 5 τύποι φαρμάκων για την συμπτωματική θεραπεία της νόσου Πάρκινσον.
1. Ντοπαμινεργικά:
Α. Λεβοντόπα: Αποτελεί την πιο διαδεδομένη, αποτελεσματική και ωφέλιμη φαρμακευτική ουσία για την νόσο του Πάρκινσον. Είναι το πρόδρομο μόριο της Ντοπαμίνης. Χορηγείται παράλληλα με καρβιντόπα ,ώστε η μεγαλύτερη ποσοτητα της να διαπεράσει τον αιματοεγκεφαλικό φραγμό και να κατευθυνθεί στην μέλαινα ουσία για την σύνθεση ντοπαμίνης και να μην συνδεθεί σε περιφερικούς ντοπαμινεργικούς υποδοχείς δημιουργώντας αρκετές ανεπιθύμητες ενέργειες. Στις ανεπιθύμητες ενέργειες ανήκουν η ναυτία, ο έμετος , η ορθοστατική υπόταση κ.τ.λ. Η δόση συνήθως αυξάνεται με την πρόοδο της νόσου. Πολλά σκευάσματα υπάρχουν που συνδυάζουν καρβιντόπα- λεβοντόπα π.χ SINEMET.
Β. Αγωνιστές Ντοπαμίνης: Οι αγωνιστές ντοπαμίνης μπορούν να χρησιμοποιηθούν ως μονοθεραπεία στα αρχικά στάδια της νόσου και σε νέους ασθενείς. Υπάρχουν 2 μεγάλες κατηγορίες ντοπαμινεργικών αγωνιστών, οι D1 και D2. Οι D2 αγωνιστές φαίνεται να είναι πιο αποτελεσματικοί.Έχουν μεγαλύτερη διάρκεια δράσης ,ωστόσο όταν τα συμπτώματα οξυνθούν πρέπει να συγχορηγηθούν με λεβοντόπα-καρβιντόπα. Η ροπινιρόλη είναι ένας D2, D3 αγωνιστής , και διεγείρει τους ντοπαμινεργικούς υποδοχείς του ραβδωτού σώματος (κερκοφόρος, κέλυφος). Στις ανεπιθύμητες ενέργειες συγκαταλέγονται οι παρορμήσεις και οι ψυχιατρικές εκδηλώσεις. Επιπλέον, μπορεί να παρουσιαστούν ζωηρά όνειρα , ψευδαισθήσεις, παραισθήσεις.
2. Αντιχολινεργικά:
Αποτελούν παλαιότερες μορφές θεραπείας. Είναι ανταγωνιστές των μουσκαρινικών υποδοχέων και ανταγωνίζονται την μεταφορά ακετυλοχολίνης μέσω των ενδιάμεσων νευρώνων του ραβδωτού σώματος. Είναι πιο αποτελεσματικά στην αντιμετώπιση του μυϊκού τρόμου.
3. Αναστολείς ΜΑΟ και COMT:
Τα ένζυμα ΜΑΟ και COMT συμμετέχουν στο μεταβολισμό τη ντοπαμίνης στη συναπτική σχισμή. Φαρμακευτικές ουσίες όπως η εντακαπόνη ,η οποία είναι αναστολέας της COMT, εμποδίζουν την διάσπαση της ντοπαμίνης. Μελέτες έχουν δείξει ότι ως μονοθεραπεία δεν είναι αποτελεσματική. Μπορεί να ενισχύσει τη δράση των Λεβοντόπα-Καρβιντόπα όταν συγχορηγείται.
4. Αμαντανίδη:
Η αμαντανίδη είναι ένας αντιικός παράγοντας. Βρέθηκε τυχαία ότι λειτουργεί και ως NMDA ανταγωνιστής.Η αμανταδίνη φαίνεται ότι έχει μία ήπια επίδραση στην αντιμετώπιση του μυϊκού τρόμου.
Πέρα από τις κινητικές διαταραχές τα άτομα με Πάρκινσον κατακλύζονται και από ψυχιατρικές διαταραχές.
Η κατάθλιψη μπορεί να αντιμετωπιστεί με τη χορήγηση αναστολέων επαναπρόσληψης σεροτονίνης SSRIs ή τρικυκλικών αντικαταθλιπτικών π.χ Amitriptyline. Η ηλεκτροσπασμοθεραπεία προτείνεται σε περιπτώσεις που δεν μπορούν να χορηγηθούν από του στόματος τα φάρμακα. Αν ο ασθενής παρουσιάζει ψύχωση λόγω της φαρμακευτικής αγωγής προτείνεται η χορήγηση κλοζαπίνης η οποία έχει ισχυρές αντιχολινεργικές , αντιισταμινικές, αντι α – αδρενεργικές επιδράσεις.
Ακόμα, η άνοια μπορεί να βελτιωθεί με τη χορήγηση αναστολέων ακετυλοχολινεστεράσης όπως η ριβαστιγμίνη.
Παρακάτω παρουσιάζονται και κάποιες θεραπείες που βρίσκονται σε πειραματικό στάδιο, αλλά είναι πολλά υποσχόμενες.
Θεραπεία με βλαστοκύτταρα
Μπορούν να ληφθούν εμβρυικά βλαστικά κύτταρα από τα αρχικά στάδια της βλαστοκύστης και στη συνέχεια να διαφοροποιηθούν στο εργαστήριο σε ντοπαμινεργικούς νευρώνες.
Οι ινοβλάστες λειτουργούν και αυτοί ως βλαστικά κύτταρα και μπορούν να διαφοροποιηθούν in-vitro σε ντοπαμινεργικούς νευρώνες. Αξίζει να σημειωθεί ότι η χρησιμοποίηση των ινοβλαστών ως βλαστικά κύτταρα για την αντιμετώπιση του Πάρκινσον προϋποθέτει ότι δεν περιέχουν στο γενετικό υλικό μεταλλάξεις των γονιδίων που απεικονίζονται στον Πίνακα 1.Πολλές έρευνες σε πειραματόζωα βρίσκονται σε εξέλιξη, ωστόσο η χρησιμοποίηση των βλαστικών κυττάρων παρουσιάζει αρκετές δυσκολίες για την αντιμετώπιση του Πάρκινσον.
Chaperones-Πρωτεΐνες μοριακοί συνοδοί.
Όπως έχει ήδη αναφερθεί η μη σωστή αναδίπλωση της α-συνουκλείνης μπορεί να οδηγήσει στη νόσο Πάρκινσον. Πολλές πειραματικές μελέτες τα τελευταία χρόνια επικεντρώνονται στην αύξηση της παραγωγής μοριακών συνοδών π.χ Hsp-70 ή στην χορήγησή τους. Οι πρωτεΐνες αυτές οδηγούν στη σωστή αναδίπλωση των πρωτεϊνών στο χώρο. Αναστολείς των Hsp90 αναστέλλουν την αλληλεπίδραση των Hsp-90 και του HSF1 (προσδέτης του Hsp-90) . Αυτό οδηγεί στην αύξηση της έκφρασης και της δραστηριότητας του μοριακού συνοδού Ηsp-70.
Γονιδιακή θεραπεία.
Η γονιδιακή θεραπεία είναι μία μη φαρμακολογική προσέγγιση η οποία στοχεύει στην αύξηση της έκφρασης των chaperones. Ένας αδενοιός μολύνει τον ασθενή στον οποίο έχουν εισαχθεί γονίδια που επάγουν την έκφραση μοριακών συνοδών π.χ Hsp70,Hsp-90. Παράλληλα, οι ιοί αυτοί περιέχουν γονίδια που παράγουν νευροτροφικούς παράγοντες (NGF) και ένζυμα που ενισχύουν την έκκριση ντοπαμίνης.
Ανοσοθεραπεία
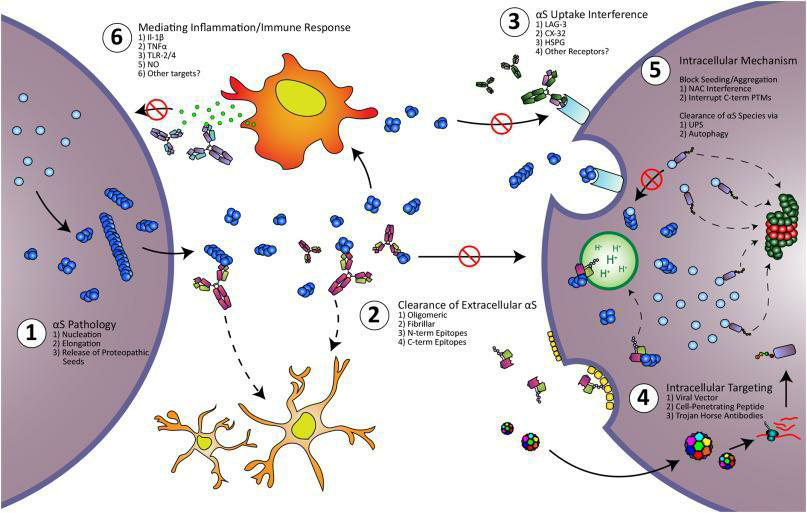
Είναι μέθοδος που χρησιμοποιεί αντισώματα για την αναστολή συγκεκριμένων μορίων, επιτόπων. Πρωταρχικός στόχος των αντισωμάτων είναι να στραφούν εναντιων των συσσωματωμάτων α συνουκλείνης και να απομακρυνθούν ύστερα από την ενεργοποίηση των μικρογλοιακών (1). Αντισώματα μπορεί να στραφούν και εναντίων μεμβρανικών πρωτεϊνών που συμμετέχουν στην επαναπρόσληψη της α συνουκλείνης (2). Τέλος , αντισώματα μπορούν να στοχευθούν και σε μεσολαβητές της φλεγμονής (π.χ κυτταροκίνες) μειώνοντας την φλεγμονώδη απόκριση των μικρογλοιακών (3). Το σχήμα δείχνει τις πιθανές δράσεις των αντισωμάτων.
Χειρουργική θεραπεία
Η χειρουργικής θεραπεία ενδείκνυται όταν η φαρμακευτική αγωγή δεν επιφέρει πλέον αποτελέσματα στην νόσο Πάρκινσον. Η πιο διαδεδομένη χειρουργική θεραπεία είναι η εν τω βάθει εγκεφαλική διέγερση (DBS). Αυτή μειώνει τα συμπτώματα της νόσου Πάρκινσον και βελτιώνει την ποιότητα ζωής των ασθενών. Οι δυο στόχοι της εγκεφαλικής διέγερσης είναι ο υποθαλαμιος πυρήνας (STN) και η έσω ωχρά σφαίρα (GPi). Πολλές μελέτες έχουν συνταχθεί με σκοπό να αποδείξουν την αποτελεσματικότητα της εγκεφαλικής διέγερσης. Οι περισσότερες καταλήγουν ότι τόσο η διέγερση του STN όσο της GPi έχουν τα ίδια και άμεσα αποτελέσματα.

Παρόλη την εγκεφαλική διέγερση μπορεί να συνεχίζεται η φαρμακευτική αγωγή, αλλά σε χαμηλότερες δόσεις. Η διάρκεια λειτουργίας της μπαταρίας του νευροδιεγέρτη κυμαίνεται από 5 με 10 χρόνια ανάλογα την εταιρία, όπου και αντικαθίσταται .
Στερεοτακτική ακτινοχειρουργική
Είναι μια ελάχιστα επεμβατική ,εξαιρετικά ακριβής και ανώδυνη μέθοδος που στοχεύει στην αντιμετώπιση κυρίως του μυϊκού τρόμου. Μέσω λεπτών ακτίνων γ (γ-knife) στοχεύεται ο διάμεσος κοιλιακός πυρήνας του θαλάμου , ο οποίος συμμετέχει στη δημιουργία του τρόμου ηρεμίας. Σε μια μελέτη των Sudesh S Raju et al. που πραγματοποιήθηκε σε 33 ασθενεις με νόσο Πάρκινσον διαπιστώθηκε ότι το 93.9% των ασθενών (31 ασθενείς) που υποβλήθηκε σε στερεοτακτική ακτινοχειρουργική παρουσίασε σημαντική βελτίωση του τρόμου ηρεμίας. Πρόκειται για μια αρκετά ασφαλή και αποτελεσματική μέθοδο η οποία ενδείκνυται κυρίως στους ηλικιωμένους και στους ασθενείς που δεν μπορεί να γίνει εφικτή η εν τω βάθη εγκεφαλική διέγερση (DBS).

Φυσικοθεραπευτικές παρεμβάσεις
Οι φυσικοθεραπευτικές παρεμβάσεις στοχεύουν στην αύξηση του επιπέδου λειτουργικότητας των ασθενών με νόσο Parkinson. Επιπλέον, στοχεύουν στην βελτίωση των κλινικών σημείων της νόσου, όπως η διαταραχή της ισορροπίας και της βάδισης.
Μελέτες έδειξαν ότι η άσκηση πάνω σε διάδρομο υποστηριζόμενου σωματικού βάρους με κινηματική καταγραφή, συμβάλλει στην βελτίωση του διασκελισμού και της ταχύτητας.
Επιπρόσθετα, ο χρόνος διατήρησης της όρθιας θέσης διπλασιάστηκε καθώς και ο φόβος πτώσεων μειώθηκε εξίσου σημαντικά.
Η χρήση εξωτερικών ερεθισμάτων σε συνδυασμό με θεραπευτικές ασκήσεις φαίνεται να έχει ευεργετική επίδραση, αφού τα σωματοαισθητικά ερεθίσματα παρακάμπτουν τα αλλοιωμένα βασικά γάγγλια, έχοντας ως αποτέλεσμα τη χρήση άλλων νευρικών οδών. Πιο συγκεκριμένα, τα ακουστικά ερεθίσματα βελτιώνουν σε μεγάλο βαθμό την ταχύτητα, το ρυθμό και το μήκος βήματος. Ταυτόχρονα, τα οπτικά ευοδώνουν την ταχύτητα στροφής, αυξάνουν την ώθηση και βελτιώνουν την έναρξη βάδισης.
Ύστερα από συστηματική ανάλυση παρατηρήθηκε ότι η ταυτόχρονη χρήση οπτικών και ακουστικών ερεθισμάτων ήταν λιγότερο αποτελεσματική από όταν χρησιμοποιήθηκαν ξεχωριστά.
Εξαιτίας της μυϊκής αδυναμίας που εμφανίζουν οι ασθενείς με νόσο Parkinson, στο πρόγραμμα αποκατάστασης θα πρέπει να εντάσσονται ασκήσεις αντίστασης, καθώς φαίνεται να βελτιώνουν τα ελλείμματα κινητικής λειτουργίας, την ποιότητα ζωής, την δύναμη των μυών αλλά και το φόβο για πτώση.
Παρότι η αστάθεια της στάση αποτελεί ένα μείζον πρόβλημα για τους ασθενείς, στο ασκησιολόγιο κρίνεται ωφέλιμη η έμφαση στις προοδευτικές ασκήσεις ισορροπίας. Αναλυτικότερα, η ισορροπία μονοποδικής στήριξης στην μετάβαση σε μονοποδική στήριξη πάνω σε bosu, φαίνεται να έχει ευεργετικά αποτελέσματα σε ασθενείς που πάσχουν από ήπιο έως και μέτριο Parkinson. Συμπληρωματικά, αξίζει να χρησιμοποιηθούν και εναλλακτικές μορφές θεραπείας όπως είναι η χοροθεραπεία και το taichi.
Βιβλιογραφία:
1. Kouli, A., Torsney, K. M., & Kuan, W.-L. (2018). Parkinson’s Disease: Etiology, Neuropathology, and Pathogenesis. In Parkinson’s Disease: Pathogenesis and Clinical Aspects (pp. 3–26). Codon Publications.
2. Mana R. Ehlers, & Rebecca M. Todd. (2017). Genesis and Maintenance of Attentional Biases: The Role of the Locus Coeruleus-Noradrenaline System. Neural Plasticity, 1(1), 2–3.
3. Tan, E. K., Chao, Y. X., West, A., Chan, L. L., Poewe, W., & Jankovic, J. (2020, June 1). Parkinson disease and the immune system — associations, mechanisms and therapeutics. Nature Reviews Neurology. Nature Research.
4. Li, X., Sundquist, J., & Sundquist, K. (2012). Subsequent risks of Parkinson disease in patients with autoimmune and related disorders: A nationwide epidemiological study from Sweden. Neurodegenerative Diseases, 10(1–4), 277–284.
5. Stoker, T. B. (2018). Stem Cell Treatments for Parkinson’s Disease. In Parkinson’s Disease: Pathogenesis and Clinical Aspects (pp. 161–175). Codon Publications.
6. Mana R. Ehlers, & Rebecca M. Todd. (2017). Genesis and Maintenance of Attentional Biases: The Role of the Locus Coeruleus-Noradrenaline System. Neural Plasticity, 1(1), 2–3.
7. Schwab, A. D., Thurston, M. J., Machhi, J., Olson, K. E., Namminga, K. L., Gendelman, H. E., & Mosley, R. L. (2020, April 1). Immunotherapy for Parkinson’s disease. Neurobiology of Disease. Academic Press Inc.
8. Lee, D., Dallapiazza, R., De Vloo, P., & Lozano, A. (2018, August 1). Current surgical treatments for Parkinson’s disease and potential therapeutic targets. Neural Regeneration Research. Wolters Kluwer Medknow Publications.
9. Frank H. Netter. Παθολογία Νευρικό Σύστημα. 4η έκδοση. Εκδόσεις Π.Χ Πασχαλίδης
10. Harrison. Νευρολογία στην Κλινική Ιατρική. 2η έκδοση. εκδόσεις Παρισιάνου
11. Daroff. Bradley’s neurology in clinical Practice. 7th edition. ELSEVIER
12. ΕΥΡΩΠΑΙΚΗ ΚΟΙΝΗ ΔΙΑΚΗΡΥΞΗ ΓΙΑ ΤΑ ΠΡΟΤΥΠΑ ΦΡΟΝΤΙΔΑΣ ΣΤΗ ΝΟΣΟ ΠΑΡΚΙΝΣΟΝ source: https://socialpolicy.gr/2017/04/ευρωπαϊκή-κοινή-διακήρυξη-για-τα-πρότ.html
13. TYPES OF PARKINSONSMS source: https://www.parkinson.org/Understanding-Parkinsons/What-is-Parkinsons/Types-of-Parkinsonisms
14. TYPES OF PARKINSON’S AND PARKINSONISM source: https://www.epda.eu.com/about-parkinsons/types/
15. TYPES OF PARKINSON’S DISEASE source: https://parkinsonsnewstoday.com/types-of-parkinsons-disease/
16. Duffy J., (2012). Νευρογενείς κινητικές διαταραχές ομιλίας υποστρώματα, διαφορική διάγνωση & αντιμετώπιση, Επιμέλεια Γρηγόριος Νάσιος & Μαρία Ιγνατίου, εκδόσεις Π.Χ. Πασχαλίδης Αθήνα
17. Kakkar, A.K., and Dahiya, N. (2015). Management of Parkinsons disease: Current and future pharmacotherapy. European journal of pharmacology 750, 74-81.
18. Schulman LM, Taback RL, Rabinstein AA, Weiner WJ. (2002). Nonrecognition of depression and other non-motor symptoms in Parkinson’s disease. Parkinsonism Related Disord; 8:193-197
19. Suzanne “Tink” Martin, Mary Kessler. Φυσικοθεραπευτικές παρεμβάσεις σε ασθενείς με νευρολογικές παθήσεις. Κωνσταντάρας Ιατρικές Εκδόσεις. ISBN: 978-960-6802-74-4
20. Deborah Nichols-Larsen. Νευρολογική Αποκατάσταση Νευροεπιστήμη και Νευροπλαστικότητα στην Εφαρμοσμένη Φ/Θ. Κωνσταντάρας Ιατρικές Εκδόσεις. ISBN: 9789606802997
21. George DeMaagd, PharmD, BCPS and Ashok Philip, PhD. (2015). Parkinson’s Disease and Its Management Part 1: Disease Entity, Risk Factors, Pathophysiology, Clinical Presentation, and Diagnosis. 2015 Aug; 40(8): 504-510, 532.
22. Cano-de-la-Cuerda R, Pérez-de-Heredia M, Miangolarra-Page JC, Muñoz-Hellín E, Fernández-de-Las-Peñas C. Is there muscular weakness in Parkinson’s disease? Am J Phys Med Rehabil. 2010 Jan;89(1):70-6
23. Dibble LE, Hale TF, Marcus RL, Gerber JP, LaStayo PC. High intensity eccentric resistance training decreases bradykinesia and improves Quality Of Life in persons with Parkinson’s disease: a preliminary study. Parkinsonism Relat Disord. 2009 Dec;15(10):752-7
24. Ebersbach G, Edler D, Kaufhold O, Wissel J. Whole body vibration versus conventional physiotherapy to improve balance and gait in Parkinson’s disease. Arch Phys Med Rehabil. 2008 Mar;89(3):399-403.
25. Falvo, M. J., B. K. Schilling and G. M. Earhart (2008). “Parkinson’s disease and resistive exercise: rationale, review, and recommendations.” Mov Disord 23(1): 1-11.
26. Fisher, B. E., A. D. Wu, G. J. Salem, J. Song, C. H. Lin, J. Yip, S. Cen, J. Gordon, M. Jakowec and G. Petzinger (2008). “The effect of exercise training in improving motor performance and corticomotor excitability in people with early Parkinson’s disease.” Arch Phys Med Rehabil 89(7): 1221-1229.
27. Franzen, E., C. Paquette, V. S. Gurfinkel, P. J. Cordo, J. G. Nutt and F. B. Horak (2009). “Reduced performance in balance, walking and turning tasks is associated with increased neck tone in Parkinson’s disease.” Exp Neurol 219(2): 430-438.
28. Jankovic, J. (1999). “New and emerging therapies for Parkinson disease.” Arch Neurol 56(7): 785-790.
29. Jankovic, J. (2002). “Essential tremor: a heterogenous disorder.” Mov Disord 17(4): 638-644.
30. Louis, E. D. and E. C. Jurewicz (2003). “Olfaction in essential tremor patients with and without isolated rest tremor.” Mov Disord 18(11): 1387-1389.
31. Mehrholz J, Friis R, Kugler J, Twork S, Storch A, Pohl M. Treadmill training for patients with Parkinson’s disease. Cochrane Database Syst Rev. 2010 Jan 20;(1):CD007830.
32. Michalowska, M., U. Fiszer, A. Krygowska-Wajs and K. Owczarek (2005). “Falls in Parkinson’s disease. Causes and impact on patients’ quality of life.” Funct Neurol 20(4): 163-168.
33. Miyai, I., Y. Fujimoto, Y. Ueda, H. Yamamoto, S. Nozaki, T. Saito and J. Kang (2000). “Treadmill training with body weight support: its effect on Parkinson’s disease.” Arch Phys Med Rehabil 81(7): 849-852.
34. Nieuwboer, A. and N. Giladi (2008). “The challenge of evaluating freezing of gait in patients with Parkinson’s disease.” Br J Neurosurg 22 Suppl 1: S16-18.
35. Nieuwboer, A., K. Baker, A. M. Willems, D. Jones, J. Spildooren, I. Lim, G. Kwakkel, E. Van Wegen and L. Rochester (2009). “The short-term effects of different cueing modalities on turn speed in people with Parkinson’s disease.” Neurorehabil Neural Repair 23(8): 831-836.
36. Palo-Bengtsson, L. and S. L. Ekman (1997). “Social dancing in the care of persons with dementia in a nursing home setting: a phenomenological study.” Sch Inq Nurs Pract 11(2): 101-118; discussion 119-123.
37. Rochester, L., A. Nieuwboer, K. Baker, V. Hetherington, A. M. Willems, F. Chavret, G. Kwakkel, E. Van Wegen, I. Lim and D. Jones (2007). “The attentional cost of external rhythmical cues and their impact on gait in Parkinson’s disease: effect of cue modality and task complexity.” J Neural Transm (Vienna) 114(10): 1243-1248.
38. Rochester, L., D. Rafferty, C. Dotchin, O. Msuya, V. Minde and R. W. Walker (2010). “The effect of cueing therapy on single and dual-task gait in a drug naive population of people with Parkinson’s disease in northern Tanzania.” Mov Disord 25(7): 906-911.
39. Schenkman, M., T. M. Cutson, M. Kuchibhatla, J. Chandler, C. F. Pieper, L. Ray and K. C. Laub (1998). “Exercise to improve spinal flexibility and function for people with Parkinson’s disease: a randomized, controlled trial.” J Am Geriatr Soc 46(10): 1207-1216.
TrueMed-ForLivingMore
Κοινοποιήστε


Ιωάννης Κουκουλίθρας
Συντάκτης
O Ιωάννης Κουκουλίθρας είναι τριτοετής φοιτητής ιατρικής του Πανεπιστημίου Ιωαννίνων. Τα ενδιαφέροντά του επικεντρώνονται στη νευροφυσιολογία και αντιμετώπιση του χρόνιου πόνου, στις νευρολογικές παθήσεις , στις διαταραχές ύπνου και στις μυοσκελετικές παθήσεις. Έχει συμμετάσχει σε πολλά νευρολογικά και ορθοπεδικά συνέδρια. Είναι κάτοχος BLS, B-CON από το 2018 του Ευρωπαϊκού Συμβουλίου Αναζωογόνησης. Είναι μέλος της Αμερικανικής Ακαδημίας Νευρολογίας (American Academy of Neurology,AAN). Είναι βοηθός του εργαστηρίου Ανατομίας , Ιστολογίας, Εμβρυολογίας της Ιατρικής του Παν. Ιωαννίνων. Έχει μέχρι στιγμής (28/3/2020) 3 επιστημονικές δημοσιεύσεις.
Σπυρίδων Κολοκώτσιος
Συντάκτης
Ο Σπυρίδων Κολοκώτσιος είναι φοιτητής στο 4ο ακαδημαϊκό έτος του Πανεπιστημίου Δυτικής Αττικής του τμήματος Φυσικοθεραπείας.Τα ενδιαφέροντα του βασίζονται στην αντιμετώπιση του χρόνιου πόνου και στις μυοσκελετικές διαταραχές. Είναι πιστοποιημένος ως CKTP και έχει συμμετάσχει σε πληθώρα σεμιναρίων εκ των οποίων μερικά από αυτά είναι: Arthro tools Instrument Assisted Soft Tissue Mobilization,Kinesio Taping Assessments Fundamental Concepts and Techniques – International, Kinesio Taping Clinical Reasoning and Advanced Techniques, Mention Prevention
Αλεξάνδρα Σταμούλη
Συντάκτρια
Η Αλεξάνδρα Σταμούλη εισήχθη 8η στο Τμήμα Φυσικοθεραπείας του Πανεπιστημίου Δυτικής Αττικής και φοιτεί στο 4ο ακαδημαϊκό έτος. Στόχο της αποτελεί η ενασχόληση πάνω στην αντιμετώπιση μυοσκελετικών και νευρολογικών παθήσεων και η έρευνα για την ανάπτυξη και τεκμηρίωση καινούριων φυσικοθεραπευτικών μεθόδων και τεχνικών.
Μηνάς Πλεξουσάκης
Συντάκτης
Ο Μηνάς Πλεξουσάκης είναι φοιτητής στο 4ο ακαδημαϊκό έτος του Πανεπιστημίου Δυτικής Αττικής του τμήματος Φυσικοθεραπείας. Κυρίαρχο ενδιαφέρον του είναι τα μυοσκελετικά προβλήματα και αντιμετώπιση του χρόνιου πόνου. Παράλληλα ασχολείται και με νευρολογικά περιστατικά έχοντας ως βασικό στόχο την βελτίωση της λειτουργικότητας τους μέσω εκσυγχρονισμένων προγραμμάτων φυσικοθεραπείας.
ΔΗΜΟΦΙΛΗ ΕΒΔΟΜΑΔΑΣ
ΡΟΗ ΕΙΔΗΣΕΩΝ
| Επικοινωνία | Η ομάδα μας | Διαφημιστείτε στη truemed.gr| | Όροι χρήσης | Προσωπικά δεδομένα | Copyright©Truemed | |Για περισσότερη ζωή | Υγειά-διατροφή |
Designed – Developed by Premiumweb.gr
ΒΡΕΙΤΕ ΜΑΣ ![]()

© 2019 TrueMed Media. All rights reserved. Our website services, content, and products are for informational purposes only. TrueMed Media does not provide medical advice, diagnosis, or treatment.
Parkinson: απο την αιτιοπαθογένεια στη θεραπεία
![]() 29-7-2020
29-7-2020
![]() Ιωάννης Κουκουλίθρας
Ιωάννης Κουκουλίθρας
![]() Αλεξάνδρα Σταμούλη
Αλεξάνδρα Σταμούλη
![]() Μηνάς Πλεξουσάκης
Μηνάς Πλεξουσάκης
![]() Σπυρίδων Κολοκώτσιος
Σπυρίδων Κολοκώτσιος

Ο παρκινσονισμός είναι ένας ευρύς όρος που μελετά το σύνολο των σημείων και των συμπτωμάτων που χαρακτηρίζουν τη νόσο του Parkinson.
Τον πιο συχνό τύπο παρκινσονισμού, περίπου το 80-85% των περιπτώσεων ,αποτελεί ο ιδιοπαθής/πρωτοπαθής παρκινσονισμός ή νόσος του Parkinson. Ο τύπος αυτός αποκρίνεται καλά στα φάρμακα τα οποία έχουν ως σκοπό την αύξηση ή υποκατάσταση της ντοπαμίνης.
Το υπόλοιπο 10-15% των περιπτώσεων αποτελεί ο δευτεροπαθής/άτυπος παρκινσονισμός , ο οποίος είναι απόρροια άλλων παθήσεων και πιθανώς σχετίζεται με εγκεφαλίτιδα, αλκοολισμό, έκθεση σε ορισμένες τοξικές ουσίες, κρανιοεγκεφαλικές κακώσεις, αγγειακά εγκεφαλικά επεισόδια (Vascular parkinsonism) και χρήση ψυχοτρόπων φαρμάκων ( Drug-induced Parkinsonism). Είναι δύσκολο να γίνει η διαφοροποίησή τους από τον πρωτοπαθή παρκινσονισμό.
Τα σύνδρομα Parkinson’s Plus αποτελούν ένα σύνολο παθήσεων-διαταραχών που εκδηλώνονται σαν την νόσο του Parkinson. Ασθενείς με δευτεροπαθή παρκινσονισμό δεν ανταποκρίνονται καλά σε ντοπαμινεργικές φαρμακευτικές αγωγές, όπως για παράδειγμα η Levodopa και είναι πιο δύσκολη η αντιμετώπιση από αυτούς με νόσο του Parkinson. Τέτοια σύνδρομα αποτελούν:
· η ατροφία πολλαπλών συστημάτων (Multiple System Atrophy ή MSA)
· η προοδευτική υπερπυρηνική παράλυση (Progressive Supranuclear Palsy ή PSP)
· το κορτικοβασικό σύνδρομο (Corticobasal Syndrome ή CBS)
Στα σύνδρομα Parkinson’s Plus εκτός από τα συμπτώματα που οφείλονται στην εκφύλιση της μέλαινας ουσίας, συνυπάρχουν και άλλα νευρολογικά σημεία που σχετίζονται με την δυσλειτουργία της παρεγκεφαλίδας και του αυτονόμου νευρικού συστήματος.
Νόσος Parkinson
Η νόσος Parkinson όπως περιγράφηκε για πρώτη φορά από τον James Parkinson το 1817 είναι η δεύτερη πιο συχνή νευροεκφυλιστική νόσος (μετά τη νόσο Alzheimer) η οποία χαρακτηρίζεται από βραδυκινησία, δυσκαμψία , τρόμο ηρεμίας , συρόμενο βάδισμα, παγωμένο προσωπείο. Προσβάλλει περισσότερο από 1 εκατομμύριο άτομα στην Ευρώπη και το οικονομικό αντίκτυπο της νόσου είναι τεράστιο. Εκτιμάται περίπου σε 13,3 δις στην Ευρώπη το έτος. Το 2003 στο Ηνωμένο βασίλειο το ετήσιο κόστος φροντίδας για κάθε ασθενή με νόσο Πάρκινσον ήταν 9.975 Ευρώ. Η έναρξη των συμπτωμάτων εκτιμάται τα 40-70 έτη με κορύφωση τα 60 έτη. Η πορεία της νόσου κυμαίνεται από 10 έως 25 έτη.
Πρόκειται για μία διαταραχή του εξωπυραμιδικού συστήματος και συγκεκριμένα του κυκλώματος των βασικών γαγγλίων το οποίο ρυθμίζεται από την παρουσία ντοπαμίνης. Παρατηρείται εκφύλιση των ντοπαμινεργικών νευρώνων της συμπαγούς μοίρας της μέλαινας ουσίας στο μέσο εγκέφαλο με ταυτόχρονη προσβολή της μελαινο-ραβδωτής οδού. Το κύκλωμα των βασικών γαγγλίων το οποίο αποτελείται ανατομικά από τον κερκοφόρο π. , το κέλυφος , την ωχρά σφαίρα , προτείχισμα , αμυγδαλοειδή π. συμμετέχει στον έλεγχο των κινήσεων, των μεμαθημένων κινήσεων και της στάσης. Αποτελείται από GABA εργικούς νευρώνες(ανασταλτικούς) , με εξαίρεση των υποθαλάμιο πυρήνα ο οποίος είναι Glutaminergic (διεγερτικός) Το κύκλωμα αυτό διαχωρίζεται σε άμεσο διεγερτικό και έμμεσο ανασταλτικό. Το σχήμα 1 παρουσιάζει τις συνδέσεις του κυκλώματος αυτού σε φυσιολογικές συνθήκες και στη νόσο Parkinson. Στην νόσο Parkinson, λόγω της ντοπαμινεργικής εκφύλισης υπολειτουργεί το άμεσο διεγερτικό κύκλωμα και υπερλειτουργεί το έμμεσο ανασταλτικό , με αποτέλεσμα να μην στέλνονται ώσεις στους πυρήνες του θαλάμου(οπίσθιοι κοιλιακοί πλάγιοι) , οι οποίοι με την σειρά τους δεν στέλνουν ευοδωτικά ερεθίσματα στον κινητικό φλοιό του εγκεφάλου (π.4, π.6 Brodmann). Το αποτέλεσμα είναι κυρίως βραδυκινησία και δυσκαμψία. Να σημειωθεί ότι οι D1 υποδοχείς του ραβδωτού σώματος στο άμεσο κύκλωμα έχουν διεγερτικό ρόλο ,ενώ οι D2 υποδοχείς στο έμμεσο κύκλωμα έχουν ανασταλτικό ρόλο.

Παρά τις εντατικές έρευνες που έχουν γίνει και συνεχίζουν να γίνονται ακόμα, η ακριβής αιτιολογία της νόσου Πάρκινσον δεν είναι ακόμη γνωστή. Ποικίλοι μηχανισμοί έχουν αναφερθεί στη διεθνή βιβλιογραφία που προκαλούν εκφύλιση των ντοπαμινεργικών νευρώνων, ωστόσο αυτή της μιτοφαγίας κερδίζει όλο και περισσότερο έδαφος τα τελευταία χρόνια. Πιθανολογείται ότι υπάρχει μία πολυσύνθετη αλληλεπίδραση μεταξύ γενετικών και περιβαλλοντικών παραγόντων. Οι παράγοντες κινδύνου περιλαμβάνουν: θετικό οικογενειακό ιστορικό , άρρεν φύλο, κρανιοεγκεφαλική κάκωση, έκθεση σε εντομοκτόνα, κατανάλωση νερού από πηγές και την διαμονή στην ύπαιθρο. Τα ακριβή αίτια αναλύονται παρακάτω.
MPTP (1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine).
Το 1983 στην Καλιφόρνια των Η.Π.Α παρουσιάστηκε ραγδαία αύξηση των ατόμων που παρουσίαζαν συμπτώματα Παρκινσονισμού. Έρευνες της εποχής έδειξαν ότι ένα από τα συστατικά των ναρκωτικών ουσιών που χρησιμοποιούνταν ήταν το MPTP. Το MPTP μεταβολίζεται σε νευροτοξίνη MPP+ , η οποία είναι ένας εκλεκτικός αναστολέας του μιτοχονδριακού συμπλόκου 1 της αναπνευστικής αλυσίδας στους νευρώνες της μέλαινας ουσίας. Αυτό οδηγεί στην δημιουργία ελεύθερων ριζών, μεταλλάξεων στο μιτοχονδριακό DNA και τελικά ντοπαμινεργική εκφύλιση.
Μελέτες έχουν δείξει ότι τα επίπεδα του ελεύθερου σιδήρου είναι ταυτόχρονα αυξημένα.
Γενετικά
Παρόλο που το Πάρκινσον θεωρείται μία ιδιοπαθής νόσος μόνο το 15% των ασθενών παρουσιάζει οικογενειακό ιστορικό. 23 γονίδια έχουν συνδεθεί με τη νόσο Πάρκινσον αν και τα τελευταία χρόνια αυξάνονται.
Ο πίνακας 1 παρουσιάζει κάποια από τα γονίδια που συμμετέχουν στη νόσο Πάρκινσον.
|
Γενετική Θέση |
Γονίδιο |
Πρωτεΐνη |
Λειτουργία |
Κληρονομικότητα |
|
PARK1 |
SNCA |
α-συνουκλεΐνη |
Κυκλοφορία κυστιδίων Ντοπαμίνης |
ΑΕ |
|
PARK2 |
PRKN |
Παρκίνη |
Λιγάση Ε3 ουμπικιτίνης |
ΑΥ |
|
PARK4 |
SNCA |
α-συνουκλεΐνη |
Κυκλοφορία κυστιδίων Ντοπαμίνης |
ΑΕ |
|
PARK5 |
UCH-L1 |
UCH-L1 |
Υδροξυλάση L1 -COOH της Ουμπικιτίνης |
ΑΕ |
|
PARK6 |
PINK |
PINK 1 |
Μιτοχονδριακή κινάση |
ΑΥ |
Πίνακας 1: Παρουσιάζει τις πιο συνηθισμένες γονιδιακές μεταλλάξεις , τις επιπτώσεις τους και την κληρονομικότητα. Από Harrison, Νευρολογία στην Κλινική Ιατρική, εκδόσεις Παρισιάνος
Από τις συνηθισμένες μεταλλάξεις είναι του γονιδίου PARK1 το οποίο κωδικοποιεί την α -συνουκλεΐνη , μία πρωτεΐνη η οποία συμμετέχει στην ανακύκλωση των κυστιδίων που περιέχουν το νευροδιαβιβαστή ντοπαμίνη στους ντοπαμινεργικούς νευρώνες της μέλαινας ουσίας. Η α- συνουκλεΐνη είναι μία μη αναδιπλωμένη πρωτεΐνη. Μετάλλαξή της οδηγoούν σε λανθασμένη αναδίπλωση αυτής της πρωτείνης , δημιουργία β- πτυχωτής επιφάνειας , συσσωματωμάτων α – συνουκλεΐνη και τελικά φλεγμονή στην περιοχή με ντοπαμινεργική εκφύλιση. Στις ιστολογικές εξετάσεις παρουσιάζονται τα σωμάτια Lewy τα οποία είναι έγκλειστα α-συνουκλεΐνης χαρακτηριστικό παθολογοανατομικό στοιχείο της νόσου Πάρκινσον. Σωμάτια Lewy μπορεί να παρατηρηθούν αρχικά στους οσφρητικούς βολβούς αλλά και σε περιοχές όπως του μεταιχμιακού συστήματος, εγκεφαλικών συζυγιών , μετωπιαίου λοβού, συμπαγούς μοίρας μέλαινας ουσίας κτλ. Το σχήμα 2 δείχνει σωμάτια Lewy σε νευρικά κύτταρα της μέλαινας ουσίας.

Ουβικιτινίωση-Πρωτεάσωμα
Για την φυσιολογική λειτουργία των πρωτεϊνών είναι απαραίτητο να συντίθενται και να αναδιπλώνονται σωστά στο χώρο , μέχρι να πάρουν την τριτοταγή – τεταρτοταγή δομή τους. Πρωτεΐνες στις οποίες δεν έχει γίνει σωστή αναδίπλωση τους και οι μοριακοί συνοδοί δεν κατάφεραν να τις επιδιορθώσουν θα πρέπει να αποικοδομηθούν. Αυτό γίνεται μέσω ενός πολύπλοκου μηχανισμού στον οποίο συμμετέχει η ουβικιτινίωση- πρωτεάσωμα. Μεταλλάξεις των γονιδίων PARK5 και PARK2 τα οποία κωδικοποιούν πρωτεΐνες οι οποίες συμμετέχουν στον μηχανισμό του συστήματος ουβικιτινίωσης -πρωτεασώματος οδηγούν στη νόσο Πάρκινσον. Πιο συγκεκριμένα, η δυσλειτουργία της παρκίνης μπορεί από την μια να οδηγεί σε συνεχή και παθολογική ουβικιτινίωση πρωτεϊνών και τελικά ντοπαμινεργική εκφύλιση , και από την άλλη να μην μπορεί να κάνει ουβικιτινίωση των μεταλλαγμένων υποστρωμάτων π.χ α – συνουκλεΐνης , γεγονός που οδηγεί στην συσσώρευση του υποστρώματος (α -συνουκλεΐνης)
Μιτοχονδριακή δυσλειτουργία
Αποτελεί την πιο συχνή αιτία στην ιδιοπαθή και οικογενή νόσο Πάρκινσον. Μελέτες των μιτοχονδρίων των νευρώνων της συμπαγούς μοίρας της μέλαινας ουσίας σε ασθενείς με νόσο Πάρκινσον έχουν δείξει ότι υπάρχει έλλειψη του μιτοχονδριακού συμπλόκου 1 που συμμετέχει στην μεταφορά των ηλεκτρονίων στην αναπνευστική αλυσίδα. Αυτό οδηγεί στην δημιουργία ROS τα οποία είναι πολύ δραστικά μόρια και δημιουργούν μεταλλάξεις. Επιπλέον, μεταλλάξεις των γονιδίων PINK1 και παρκίνης τα οποία είναι απαραίτητα για την απομάκρυνση των δυσλειτουργικών μιτοχονδρίων οδηγούν στην μη φυσιολογική πορεία της διαδικασίας της μιτοφαγίας.
Το σχήμα 3 συνοψίζει τις αιτίες ντοπαμινεργικής εκφύλισης.

Αυτοανοσία και Parkinson
Νεότερες μελέτες έχουν δείξει ότι υπάρχει αυξημένη συσχέτιση της νόσου Πάρκινσον με αυτοάνοσες καταστάσεις. Μια μεγάλη επιδημιολογική μελέτη η οποία διεξήχθη στη Σουηδία και στην οποία συμμετείχαν περισσότεροι από 310.000 ασθενείς με αυτοάνοσα νοσήματα (π.χ σκλήρυνση κατά πλάκας, Hashimoto, νόσο Graves, πλάγια μυατροφική σκλήρυνση (ALS) κ.ά.) έδειξε ότι αυτοί οι ασθενείς είχαν 33% πιθανότητα να εμφανίσουν και νόσο Parkinson (Li, X., Sundquist et.al.) Ειδικότερα, ασθενείς που έπασχαν από σύνδρομο Sjögren είχαν ακόμη μεγαλύτερη πιθανότητα. Η συσχέτιση της νόσου Parkinson με αυτοάνοσες ασθένειες θα μπορούσε να εξηγηθεί εν μέρει από γενετικές παρεκκλίσεις που είναι κοινές σε αυτές τις καταστάσεις και που επηρεάζουν την ανοσολογική λειτουργία. Λοιμώξεις από την κοινή γρίπη και τον ιό του έρπητα φαίνεται να συμβάλλουν στην νόσο Parkinson. Αυτό φαίνεται να συμβαίνει, διότι κάποια ιϊκή πρωτεΐνη έχει πολύ μεγάλη ομοιότητα με την α- συνουκλεΐνη και έτσι ενεργοποιείται το ανοσοποιητικό σύστημα. Στην αρχή παρατηρείται ενεργοποίηση των μικρογλοιακών κυττάρων τα οποία λειτουργούν ως αντιγονοπαρουσιαστικά στο ΚΝΣ. Στη συνέχεια, εκκρίνουν κυτταροκίνες όπως IL-1β , ΤNFa κτλ. οι οποίες πυροδοτούν να εισέλθουν τα Τ-Λεμφοκύτταρα . Έτσι , δημιουργείται μία φλεγμονή στην περιοχή με τελικό αποτέλεσμα την καταστροφή των ντοπαμινεργικών νευρώνων.
Κάπνισμα
Έχουν γίνει εκτενείς μελέτες σχετικά με την επίδραση του καπνίσματος στην νόσο του Parkinson. Οι περισσότερες καταλήγουν στο συμπέρασμα ότι το κάπνισμα μειώνει την πιθανότητα εμφάνισης νόσου Πάρκινσον . Αυτό συμβαίνει , επειδή ενεργοποιούνται οι νικοτινικοί υποδοχείς των ντοπαμινεργικών νευρώνων και εκκρίνεται ντοπαμίνη. Επιπλέον, η έκκριση ντοπαμίνης συμμετέχει στο μηχανισμό επιβράβευσης(επικλινής πυρήνας). Μελέτες υποστηρίζουν ότι τα άτομα που πάσχουν από Πάρκινσον μπορούν πιο εύκολα να κόψουν το κάπνισμα, καθώς δεν έχουμε έκκριση ντοπαμίνης (δεν έχουμε ανταπόκριση στην παρουσία νικοτίνης), συνεπώς ο μηχανισμός επιβράβευσης μέσω του μεσο-μεταιχμιακού-ντοπαμινεργικού συστήματος δεν λειτουργεί φυσιολογικά.
Καφεΐνη
Η καφεΐνη φαίνεται ότι συμμετέχει και αυτή στην πρόληψη της νόσου Πάρκινσον. Η καφεΐνη είναι ένας α2 αδρενεργικός ανταγωνιστής ,με αποτέλεσμα να εμποδίζεται η επαναπρόσληψη κατεχολαμινών όπως νορεπινεφρίνη, επινεφρίνη, ντοπαμίνη. Ωστόσο, χρειάζονται ακόμη περισσότερες μελέτες για την επιβεβαίωση της αποτελεσματικότητάς της. Ο συνδυασμός χορήγησης οιστρογόνων και κατανάλωσης καφεΐνης στις μετεμμηνοπαυσιακές γυναίκες μειώνει ακόμη περισσότερο την πιθανότητα , καθώς τα οιστρογόνα εμποδίζουν τον μεταβολισμό της καφεΐνης.
Συμπτώματα
Σύμφωνα με νέες μελέτες πριν την εμφάνιση των κινητικών συμπτωμάτων παρατηρείται μια παροδική διαταραχή της όσφρησης και διαταραχή του σταδίου REM κατά την διάρκεια του ύπνου. Τα συμπτώματα αυτά δεν παραπέμπουν σε υποψία έναρξης της νόσου. Η εγκατάσταση της νόσου Parkinson είναι βραδεία και προοδευτική με κύριο σύμπτωμα τον τρόμο ηρεμίας ο οποίος εμφανίζεται σε 70% των ασθενών. Στα βασικά συμπτώματα περιλαμβάνονται η δυσκαμψία , η βραδυκινησία, η κόπωση και η διαταραχή ισορροπίας. Καθώς το Parkinson αποτελεί μια νευροεξελικτική νόσο επιπλέον συμπτώματα που μπορούν να εμφανιστούν είναι η δυσκαταποσία , το πάγωμα βάδισης και η διαταραχή ομιλίας. Όπως και στις περισσότερες νευρολογικές διαταραχές το άτομο μπορεί να εμφανίσει συμπτώματα από το αυτόνομο νευρικό σύστημα ( σιελόρροια, διαταραχές ούρησης, ορθοστατική υπόταση και δυσκοιλιότητα). Τέλος ψυχολογικές διαταραχές όπως άγχος και κατάθλιψη παρουσιάζονται στην πλειοψηφία των ασθενών.
Ο τρόμος ηρεμίας περιλαμβάνει μια συνεχή κίνηση υπτιασμού – πρηνισμού η οποία προσομοιάζει την κίνηση μέτρησης κερμάτων. Η εγκατάσταση ξεκινάει στο ένα χέρι με συχνότερο να είναι το αριστερό και κατα την διάρκεια εξέλιξης της νόσου προσβάλλεται και το άλλο. Χαρακτηριστικό του τρόμου ηρεμίας είναι ότι εξαφανίζεται με την εκούσια κίνηση και κατα την διάρκεια του ύπνου.
Λόγω της εξωπυραμιδικής υπερτονίας παρατηρείται δυσκαμψία, η οποία εκδηλώνεται ως αντίσταση στην παθητική κίνηση ως αποτέλεσμα να εμφανίζονται βραχύνσεις, με την πιο επιρρεπή μυϊκή ομάδα να είναι οι καμπτήρες του γόνατος.
Ως βραδυκινησία ορίζεται η καθυστερημένη έναρξη και η μειωμένη ταχύτητα εκτέλεσης των κινήσεων, ειδικότερα των αυτοματοποιημένων όπως η βάδιση.
Διαταραχές της ισορροπίας εκδηλώνονται με την πρόοδο της νόσου λόγω μειωμένης ανταπόκρισης των αντανακλαστικών της στάσης με αποτέλεσμα οι ασθενείς να παρουσιάζουν αυξημένη τάση προς πτώση. Επιπλέον, έχει παρατηρηθεί ότι ύστερα από την πρώτη πτώση η πιθανότητα για μεταγενέστερες αυξάνεται.
Το Πάγωμα βάδισης αποτελεί σύμπτωμα της φυσικής εξέλιξης της νόσου και εκδηλώνεται ως επεισόδιο ακινησίας κυρίως όταν ο ασθενής επιχειρεί να στρίψει τον κορμό του ή να περάσει μέσα από έναν στενό χώρο όπως μια πόρτα. Για την αντιμετώπιση του παγώματος συνιστώνται ακουστικές υποδείξεις.
Διάγνωση και Κλινική εξέταση
Η διάγνωση της νόσου βασίζεται κυρίως στην ύπαρξη 2 ή περισσότερων βασικών συμπτωμάτων (δυσκαμψία, βραδυκινησία, τρόμος ηρεμίας, διαταραχή ισορροπίας), στον αποκλεισμό των συνδρόμων Parkinson Plus και στην ανταπόκριση στην λεβοντόπα.
Στα κλινικά ευρήματα παρατηρείται ανέκφραστο πρόσωπο, στάση πρόσθιας κλίσης κορμού, κάμψη άνω άκρων στους αγκώνες και στους καρπούς, ελαφριά κάμψη των ισχίων και των γονάτων, μικρά και μπερδεμένα βήματα, επιταχυνόμενη βάδιση, μικρογραφία, μονότονη ομιλία και απουσία αιώρησης άνω άκρων κατά την βάδιση.

Προδιαθεσικοί παράγοντες
|
Αυξημένη χοληστερόλη |
Αυξημένο BMI |
Ιογενείς λοιμώξεις |
|
Έκθεση σε περιβαλλοντικές τοξίνες |
Φλεγμονή που σχετίζεται με ενεργοποίηση μικρογλοικών κυττάρων |
Διαταραχή μηχανισμών απόπτωσης |
|
κρανιοεγκεφαλικές κακώσεις |
χρήση ναρκωτικών ουσιών |
Αλκοολισμός |
|
Υψηλή θερμιδική πρόσληψη |
Μιτοχονδριακή δυσλειτουργία |
Όγκος στα βασικά γάγγλια και στον μετωπιαίο λοβό |
Αντιμετώπιση
Στόχος της θεραπείας στη νόσο Πάρκινσον είναι η διατήρηση της λειτουργικότητας και της ποιότητας ζωής του ασθενούς. Η συμπτωματική θεραπεία είναι αρκετά αποτελεσματική στην αντιμετώπιση του τρόμου ηρεμίας, βραδυκινησίας , δυσκαμψίας. Τα νοητικά συμπτώματα και οι ψυχικές διαταραχές που μπορεί να ακολουθούν δεν μπορούν να αντιμετωπιστούν με την φαρμακευτική αγωγή για την αντιμετώπιση του Πάρκινσον. Πολλές διαφορετικές απόψεις υπάρχουν για την χρονική στιγμή που πρέπει να ξεκινήσει η θεραπεία. Πολλοί πιστεύουν ότι η θεραπεία πρέπει να καθυστερήσει όσο δυνατόν περισσότερο , καθώς τα φάρμακα δεν μπορούν να φέρουν κανένα αποτέλεσμα μετά από κάποιο διάστημα και μπορεί να επιβαρύνουν την κατάσταση ακόμη περισσότερο. Ωστόσο, μοντέρνες απόψεις τονίζουν ότι η θεραπεία θα πρέπει να ξεκινήσει το συντομότερο δυνατόν για την διατήρηση επαρκούς επιπέδου νοητικής και σωματικής δραστηριότητας. Η φαρμακευτική αγωγή σε συνδυασμό με ένα κατάλληλο και εξατομικευμένο πρόγραμμα φυσικοθεραπείας αποτελούν θεραπεία εκλογής για τη νόσο Πάρκινσον.
Υπάρχουν 5 τύποι φαρμάκων για την συμπτωματική θεραπεία της νόσου Πάρκινσον.
1. Ντοπαμινεργικά:
Α. Λεβοντόπα: Αποτελεί την πιο διαδεδομένη, αποτελεσματική και ωφέλιμη φαρμακευτική ουσία για την νόσο του Πάρκινσον. Είναι το πρόδρομο μόριο της Ντοπαμίνης. Χορηγείται παράλληλα με καρβιντόπα ,ώστε η μεγαλύτερη ποσοτητα της να διαπεράσει τον αιματοεγκεφαλικό φραγμό και να κατευθυνθεί στην μέλαινα ουσία για την σύνθεση ντοπαμίνης και να μην συνδεθεί σε περιφερικούς ντοπαμινεργικούς υποδοχείς δημιουργώντας αρκετές ανεπιθύμητες ενέργειες. Στις ανεπιθύμητες ενέργειες ανήκουν η ναυτία, ο έμετος , η ορθοστατική υπόταση κ.τ.λ. Η δόση συνήθως αυξάνεται με την πρόοδο της νόσου. Πολλά σκευάσματα υπάρχουν που συνδυάζουν καρβιντόπα- λεβοντόπα π.χ SINEMET.
Β. Αγωνιστές Ντοπαμίνης: Οι αγωνιστές ντοπαμίνης μπορούν να χρησιμοποιηθούν ως μονοθεραπεία στα αρχικά στάδια της νόσου και σε νέους ασθενείς. Υπάρχουν 2 μεγάλες κατηγορίες ντοπαμινεργικών αγωνιστών, οι D1 και D2. Οι D2 αγωνιστές φαίνεται να είναι πιο αποτελεσματικοί.Έχουν μεγαλύτερη διάρκεια δράσης ,ωστόσο όταν τα συμπτώματα οξυνθούν πρέπει να συγχορηγηθούν με λεβοντόπα-καρβιντόπα. Η ροπινιρόλη είναι ένας D2, D3 αγωνιστής , και διεγείρει τους ντοπαμινεργικούς υποδοχείς του ραβδωτού σώματος (κερκοφόρος, κέλυφος). Στις ανεπιθύμητες ενέργειες συγκαταλέγονται οι παρορμήσεις και οι ψυχιατρικές εκδηλώσεις. Επιπλέον, μπορεί να παρουσιαστούν ζωηρά όνειρα , ψευδαισθήσεις, παραισθήσεις.
2. Αντιχολινεργικά:
Αποτελούν παλαιότερες μορφές θεραπείας. Είναι ανταγωνιστές των μουσκαρινικών υποδοχέων και ανταγωνίζονται την μεταφορά ακετυλοχολίνης μέσω των ενδιάμεσων νευρώνων του ραβδωτού σώματος. Είναι πιο αποτελεσματικά στην αντιμετώπιση του μυϊκού τρόμου.
3. Αναστολείς ΜΑΟ και COMT:
Τα ένζυμα ΜΑΟ και COMT συμμετέχουν στο μεταβολισμό τη ντοπαμίνης στη συναπτική σχισμή. Φαρμακευτικές ουσίες όπως η εντακαπόνη ,η οποία είναι αναστολέας της COMT, εμποδίζουν την διάσπαση της ντοπαμίνης. Μελέτες έχουν δείξει ότι ως μονοθεραπεία δεν είναι αποτελεσματική. Μπορεί να ενισχύσει τη δράση των Λεβοντόπα-Καρβιντόπα όταν συγχορηγείται.
4. Αμαντανίδη:
Η αμαντανίδη είναι ένας αντιικός παράγοντας. Βρέθηκε τυχαία ότι λειτουργεί και ως NMDA ανταγωνιστής.Η αμανταδίνη φαίνεται ότι έχει μία ήπια επίδραση στην αντιμετώπιση του μυϊκού τρόμου.
Πέρα από τις κινητικές διαταραχές τα άτομα με Πάρκινσον κατακλύζονται και από ψυχιατρικές διαταραχές.
Η κατάθλιψη μπορεί να αντιμετωπιστεί με τη χορήγηση αναστολέων επαναπρόσληψης σεροτονίνης SSRIs ή τρικυκλικών αντικαταθλιπτικών π.χ Amitriptyline. Η ηλεκτροσπασμοθεραπεία προτείνεται σε περιπτώσεις που δεν μπορούν να χορηγηθούν από του στόματος τα φάρμακα. Αν ο ασθενής παρουσιάζει ψύχωση λόγω της φαρμακευτικής αγωγής προτείνεται η χορήγηση κλοζαπίνης η οποία έχει ισχυρές αντιχολινεργικές , αντιισταμινικές, αντι α – αδρενεργικές επιδράσεις.
Ακόμα, η άνοια μπορεί να βελτιωθεί με τη χορήγηση αναστολέων ακετυλοχολινεστεράσης όπως η ριβαστιγμίνη.
Παρακάτω παρουσιάζονται και κάποιες θεραπείες που βρίσκονται σε πειραματικό στάδιο, αλλά είναι πολλά υποσχόμενες.
Θεραπεία με βλαστοκύτταρα
Μπορούν να ληφθούν εμβρυικά βλαστικά κύτταρα από τα αρχικά στάδια της βλαστοκύστης και στη συνέχεια να διαφοροποιηθούν στο εργαστήριο σε ντοπαμινεργικούς νευρώνες.
Οι ινοβλάστες λειτουργούν και αυτοί ως βλαστικά κύτταρα και μπορούν να διαφοροποιηθούν in-vitro σε ντοπαμινεργικούς νευρώνες. Αξίζει να σημειωθεί ότι η χρησιμοποίηση των ινοβλαστών ως βλαστικά κύτταρα για την αντιμετώπιση του Πάρκινσον προϋποθέτει ότι δεν περιέχουν στο γενετικό υλικό μεταλλάξεις των γονιδίων που απεικονίζονται στον Πίνακα 1.Πολλές έρευνες σε πειραματόζωα βρίσκονται σε εξέλιξη, ωστόσο η χρησιμοποίηση των βλαστικών κυττάρων παρουσιάζει αρκετές δυσκολίες για την αντιμετώπιση του Πάρκινσον.
Chaperones-Πρωτεΐνες μοριακοί συνοδοί.
Όπως έχει ήδη αναφερθεί η μη σωστή αναδίπλωση της α-συνουκλείνης μπορεί να οδηγήσει στη νόσο Πάρκινσον. Πολλές πειραματικές μελέτες τα τελευταία χρόνια επικεντρώνονται στην αύξηση της παραγωγής μοριακών συνοδών π.χ Hsp-70 ή στην χορήγησή τους. Οι πρωτεΐνες αυτές οδηγούν στη σωστή αναδίπλωση των πρωτεϊνών στο χώρο. Αναστολείς των Hsp90 αναστέλλουν την αλληλεπίδραση των Hsp-90 και του HSF1 (προσδέτης του Hsp-90) . Αυτό οδηγεί στην αύξηση της έκφρασης και της δραστηριότητας του μοριακού συνοδού Ηsp-70.
Γονιδιακή θεραπεία.
Η γονιδιακή θεραπεία είναι μία μη φαρμακολογική προσέγγιση η οποία στοχεύει στην αύξηση της έκφρασης των chaperones. Ένας αδενοιός μολύνει τον ασθενή στον οποίο έχουν εισαχθεί γονίδια που επάγουν την έκφραση μοριακών συνοδών π.χ Hsp70,Hsp-90. Παράλληλα, οι ιοί αυτοί περιέχουν γονίδια που παράγουν νευροτροφικούς παράγοντες (NGF) και ένζυμα που ενισχύουν την έκκριση ντοπαμίνης.
Ανοσοθεραπεία
Είναι μέθοδος που χρησιμοποιεί αντισώματα για την αναστολή συγκεκριμένων μορίων, επιτόπων. Πρωταρχικός στόχος των αντισωμάτων είναι να στραφούν εναντιων των συσσωματωμάτων α συνουκλείνης και να απομακρυνθούν ύστερα από την ενεργοποίηση των μικρογλοιακών (1). Αντισώματα μπορεί να στραφούν και εναντίων μεμβρανικών πρωτεϊνών που συμμετέχουν στην επαναπρόσληψη της α συνουκλείνης (2). Τέλος , αντισώματα μπορούν να στοχευθούν και σε μεσολαβητές της φλεγμονής (π.χ κυτταροκίνες) μειώνοντας την φλεγμονώδη απόκριση των μικρογλοιακών (3). Το σχήμα δείχνει τις πιθανές δράσεις των αντισωμάτων.

Χειρουργική θεραπεία
Η χειρουργικής θεραπεία ενδείκνυται όταν η φαρμακευτική αγωγή δεν επιφέρει πλέον αποτελέσματα στην νόσο Πάρκινσον. Η πιο διαδεδομένη χειρουργική θεραπεία είναι η εν τω βάθει εγκεφαλική διέγερση (DBS). Αυτή μειώνει τα συμπτώματα της νόσου Πάρκινσον και βελτιώνει την ποιότητα ζωής των ασθενών. Οι δυο στόχοι της εγκεφαλικής διέγερσης είναι ο υποθαλαμιος πυρήνας (STN) και η έσω ωχρά σφαίρα (GPi). Πολλές μελέτες έχουν συνταχθεί με σκοπό να αποδείξουν την αποτελεσματικότητα της εγκεφαλικής διέγερσης. Οι περισσότερες καταλήγουν ότι τόσο η διέγερση του STN όσο της GPi έχουν τα ίδια και άμεσα αποτελέσματα.

Παρόλη την εγκεφαλική διέγερση μπορεί να συνεχίζεται η φαρμακευτική αγωγή, αλλά σε χαμηλότερες δόσεις. Η διάρκεια λειτουργίας της μπαταρίας του νευροδιεγέρτη κυμαίνεται από 5 με 10 χρόνια ανάλογα την εταιρία, όπου και αντικαθίσταται .
Στερεοτακτική ακτινοχειρουργική
Είναι μια ελάχιστα επεμβατική ,εξαιρετικά ακριβής και ανώδυνη μέθοδος που στοχεύει στην αντιμετώπιση κυρίως του μυϊκού τρόμου. Μέσω λεπτών ακτίνων γ (γ-knife) στοχεύεται ο διάμεσος κοιλιακός πυρήνας του θαλάμου , ο οποίος συμμετέχει στη δημιουργία του τρόμου ηρεμίας. Σε μια μελέτη των Sudesh S Raju et al. που πραγματοποιήθηκε σε 33 ασθενεις με νόσο Πάρκινσον διαπιστώθηκε ότι το 93.9% των ασθενών (31 ασθενείς) που υποβλήθηκε σε στερεοτακτική ακτινοχειρουργική παρουσίασε σημαντική βελτίωση του τρόμου ηρεμίας. Πρόκειται για μια αρκετά ασφαλή και αποτελεσματική μέθοδο η οποία ενδείκνυται κυρίως στους ηλικιωμένους και στους ασθενείς που δεν μπορεί να γίνει εφικτή η εν τω βάθη εγκεφαλική διέγερση (DBS).

Φυσικοθεραπευτικές παρεμβάσεις
Οι φυσικοθεραπευτικές παρεμβάσεις στοχεύουν στην αύξηση του επιπέδου λειτουργικότητας των ασθενών με νόσο Parkinson. Επιπλέον, στοχεύουν στην βελτίωση των κλινικών σημείων της νόσου, όπως η διαταραχή της ισορροπίας και της βάδισης.
Μελέτες έδειξαν ότι η άσκηση πάνω σε διάδρομο υποστηριζόμενου σωματικού βάρους με κινηματική καταγραφή, συμβάλλει στην βελτίωση του διασκελισμού και της ταχύτητας.
Επιπρόσθετα, ο χρόνος διατήρησης της όρθιας θέσης διπλασιάστηκε καθώς και ο φόβος πτώσεων μειώθηκε εξίσου σημαντικά.
Η χρήση εξωτερικών ερεθισμάτων σε συνδυασμό με θεραπευτικές ασκήσεις φαίνεται να έχει ευεργετική επίδραση, αφού τα σωματοαισθητικά ερεθίσματα παρακάμπτουν τα αλλοιωμένα βασικά γάγγλια, έχοντας ως αποτέλεσμα τη χρήση άλλων νευρικών οδών. Πιο συγκεκριμένα, τα ακουστικά ερεθίσματα βελτιώνουν σε μεγάλο βαθμό την ταχύτητα, το ρυθμό και το μήκος βήματος. Ταυτόχρονα, τα οπτικά ευοδώνουν την ταχύτητα στροφής, αυξάνουν την ώθηση και βελτιώνουν την έναρξη βάδισης.
Ύστερα από συστηματική ανάλυση παρατηρήθηκε ότι η ταυτόχρονη χρήση οπτικών και ακουστικών ερεθισμάτων ήταν λιγότερο αποτελεσματική από όταν χρησιμοποιήθηκαν ξεχωριστά.
Εξαιτίας της μυϊκής αδυναμίας που εμφανίζουν οι ασθενείς με νόσο Parkinson, στο πρόγραμμα αποκατάστασης θα πρέπει να εντάσσονται ασκήσεις αντίστασης, καθώς φαίνεται να βελτιώνουν τα ελλείμματα κινητικής λειτουργίας, την ποιότητα ζωής, την δύναμη των μυών αλλά και το φόβο για πτώση.
Παρότι η αστάθεια της στάση αποτελεί ένα μείζον πρόβλημα για τους ασθενείς, στο ασκησιολόγιο κρίνεται ωφέλιμη η έμφαση στις προοδευτικές ασκήσεις ισορροπίας. Αναλυτικότερα, η ισορροπία μονοποδικής στήριξης στην μετάβαση σε μονοποδική στήριξη πάνω σε bosu, φαίνεται να έχει ευεργετικά αποτελέσματα σε ασθενείς που πάσχουν από ήπιο έως και μέτριο Parkinson. Συμπληρωματικά, αξίζει να χρησιμοποιηθούν και εναλλακτικές μορφές θεραπείας όπως είναι η χοροθεραπεία και το taichi.
Βιβλιογραφία:
1. Kouli, A., Torsney, K. M., & Kuan, W.-L. (2018). Parkinson’s Disease: Etiology, Neuropathology, and Pathogenesis. In Parkinson’s Disease: Pathogenesis and Clinical Aspects (pp. 3–26). Codon Publications.
2. Mana R. Ehlers, & Rebecca M. Todd. (2017). Genesis and Maintenance of Attentional Biases: The Role of the Locus Coeruleus-Noradrenaline System. Neural Plasticity, 1(1), 2–3.
3. Tan, E. K., Chao, Y. X., West, A., Chan, L. L., Poewe, W., & Jankovic, J. (2020, June 1). Parkinson disease and the immune system — associations, mechanisms and therapeutics. Nature Reviews Neurology. Nature Research.
4. Li, X., Sundquist, J., & Sundquist, K. (2012). Subsequent risks of Parkinson disease in patients with autoimmune and related disorders: A nationwide epidemiological study from Sweden. Neurodegenerative Diseases, 10(1–4), 277–284.
5. Stoker, T. B. (2018). Stem Cell Treatments for Parkinson’s Disease. In Parkinson’s Disease: Pathogenesis and Clinical Aspects (pp. 161–175). Codon Publications.
6. Mana R. Ehlers, & Rebecca M. Todd. (2017). Genesis and Maintenance of Attentional Biases: The Role of the Locus Coeruleus-Noradrenaline System. Neural Plasticity, 1(1), 2–3.
7. Schwab, A. D., Thurston, M. J., Machhi, J., Olson, K. E., Namminga, K. L., Gendelman, H. E., & Mosley, R. L. (2020, April 1). Immunotherapy for Parkinson’s disease. Neurobiology of Disease. Academic Press Inc.
8. Lee, D., Dallapiazza, R., De Vloo, P., & Lozano, A. (2018, August 1). Current surgical treatments for Parkinson’s disease and potential therapeutic targets. Neural Regeneration Research. Wolters Kluwer Medknow Publications.
9. Frank H. Netter. Παθολογία Νευρικό Σύστημα. 4η έκδοση. Εκδόσεις Π.Χ Πασχαλίδης
10. Harrison. Νευρολογία στην Κλινική Ιατρική. 2η έκδοση. εκδόσεις Παρισιάνου
11. Daroff. Bradley’s neurology in clinical Practice. 7th edition. ELSEVIER
12. ΕΥΡΩΠΑΙΚΗ ΚΟΙΝΗ ΔΙΑΚΗΡΥΞΗ ΓΙΑ ΤΑ ΠΡΟΤΥΠΑ ΦΡΟΝΤΙΔΑΣ ΣΤΗ ΝΟΣΟ ΠΑΡΚΙΝΣΟΝ source: https://socialpolicy.gr/2017/04/ευρωπαϊκή-κοινή-διακήρυξη-για-τα-πρότ.html
13. TYPES OF PARKINSONSMS source: https://www.parkinson.org/Understanding-Parkinsons/What-is-Parkinsons/Types-of-Parkinsonisms
14. TYPES OF PARKINSON’S AND PARKINSONISM source: https://www.epda.eu.com/about-parkinsons/types/
15. TYPES OF PARKINSON’S DISEASE source: https://parkinsonsnewstoday.com/types-of-parkinsons-disease/
16. Duffy J., (2012). Νευρογενείς κινητικές διαταραχές ομιλίας υποστρώματα, διαφορική διάγνωση & αντιμετώπιση, Επιμέλεια Γρηγόριος Νάσιος & Μαρία Ιγνατίου, εκδόσεις Π.Χ. Πασχαλίδης Αθήνα
17. Kakkar, A.K., and Dahiya, N. (2015). Management of Parkinsons disease: Current and future pharmacotherapy. European journal of pharmacology 750, 74-81.
18. Schulman LM, Taback RL, Rabinstein AA, Weiner WJ. (2002). Nonrecognition of depression and other non-motor symptoms in Parkinson’s disease. Parkinsonism Related Disord; 8:193-197
19. Suzanne “Tink” Martin, Mary Kessler. Φυσικοθεραπευτικές παρεμβάσεις σε ασθενείς με νευρολογικές παθήσεις. Κωνσταντάρας Ιατρικές Εκδόσεις. ISBN: 978-960-6802-74-4
20. Deborah Nichols-Larsen. Νευρολογική Αποκατάσταση Νευροεπιστήμη και Νευροπλαστικότητα στην Εφαρμοσμένη Φ/Θ. Κωνσταντάρας Ιατρικές Εκδόσεις. ISBN: 9789606802997
21. George DeMaagd, PharmD, BCPS and Ashok Philip, PhD. (2015). Parkinson’s Disease and Its Management Part 1: Disease Entity, Risk Factors, Pathophysiology, Clinical Presentation, and Diagnosis. 2015 Aug; 40(8): 504-510, 532.
22. Cano-de-la-Cuerda R, Pérez-de-Heredia M, Miangolarra-Page JC, Muñoz-Hellín E, Fernández-de-Las-Peñas C. Is there muscular weakness in Parkinson’s disease? Am J Phys Med Rehabil. 2010 Jan;89(1):70-6
23. Dibble LE, Hale TF, Marcus RL, Gerber JP, LaStayo PC. High intensity eccentric resistance training decreases bradykinesia and improves Quality Of Life in persons with Parkinson’s disease: a preliminary study. Parkinsonism Relat Disord. 2009 Dec;15(10):752-7
24. Ebersbach G, Edler D, Kaufhold O, Wissel J. Whole body vibration versus conventional physiotherapy to improve balance and gait in Parkinson’s disease. Arch Phys Med Rehabil. 2008 Mar;89(3):399-403.
25. Falvo, M. J., B. K. Schilling and G. M. Earhart (2008). “Parkinson’s disease and resistive exercise: rationale, review, and recommendations.” Mov Disord 23(1): 1-11.
26. Fisher, B. E., A. D. Wu, G. J. Salem, J. Song, C. H. Lin, J. Yip, S. Cen, J. Gordon, M. Jakowec and G. Petzinger (2008). “The effect of exercise training in improving motor performance and corticomotor excitability in people with early Parkinson’s disease.” Arch Phys Med Rehabil 89(7): 1221-1229.
27. Franzen, E., C. Paquette, V. S. Gurfinkel, P. J. Cordo, J. G. Nutt and F. B. Horak (2009). “Reduced performance in balance, walking and turning tasks is associated with increased neck tone in Parkinson’s disease.” Exp Neurol 219(2): 430-438.
28. Jankovic, J. (1999). “New and emerging therapies for Parkinson disease.” Arch Neurol 56(7): 785-790.
29. Jankovic, J. (2002). “Essential tremor: a heterogenous disorder.” Mov Disord 17(4): 638-644.
30. Louis, E. D. and E. C. Jurewicz (2003). “Olfaction in essential tremor patients with and without isolated rest tremor.” Mov Disord 18(11): 1387-1389.
31. Mehrholz J, Friis R, Kugler J, Twork S, Storch A, Pohl M. Treadmill training for patients with Parkinson’s disease. Cochrane Database Syst Rev. 2010 Jan 20;(1):CD007830.
32. Michalowska, M., U. Fiszer, A. Krygowska-Wajs and K. Owczarek (2005). “Falls in Parkinson’s disease. Causes and impact on patients’ quality of life.” Funct Neurol 20(4): 163-168.
33. Miyai, I., Y. Fujimoto, Y. Ueda, H. Yamamoto, S. Nozaki, T. Saito and J. Kang (2000). “Treadmill training with body weight support: its effect on Parkinson’s disease.” Arch Phys Med Rehabil 81(7): 849-852.
34. Nieuwboer, A. and N. Giladi (2008). “The challenge of evaluating freezing of gait in patients with Parkinson’s disease.” Br J Neurosurg 22 Suppl 1: S16-18.
35. Nieuwboer, A., K. Baker, A. M. Willems, D. Jones, J. Spildooren, I. Lim, G. Kwakkel, E. Van Wegen and L. Rochester (2009). “The short-term effects of different cueing modalities on turn speed in people with Parkinson’s disease.” Neurorehabil Neural Repair 23(8): 831-836.
36. Palo-Bengtsson, L. and S. L. Ekman (1997). “Social dancing in the care of persons with dementia in a nursing home setting: a phenomenological study.” Sch Inq Nurs Pract 11(2): 101-118; discussion 119-123.
37. Rochester, L., A. Nieuwboer, K. Baker, V. Hetherington, A. M. Willems, F. Chavret, G. Kwakkel, E. Van Wegen, I. Lim and D. Jones (2007). “The attentional cost of external rhythmical cues and their impact on gait in Parkinson’s disease: effect of cue modality and task complexity.” J Neural Transm (Vienna) 114(10): 1243-1248.
38. Rochester, L., D. Rafferty, C. Dotchin, O. Msuya, V. Minde and R. W. Walker (2010). “The effect of cueing therapy on single and dual-task gait in a drug naive population of people with Parkinson’s disease in northern Tanzania.” Mov Disord 25(7): 906-911.
39. Schenkman, M., T. M. Cutson, M. Kuchibhatla, J. Chandler, C. F. Pieper, L. Ray and K. C. Laub (1998). “Exercise to improve spinal flexibility and function for people with Parkinson’s disease: a randomized, controlled trial.” J Am Geriatr Soc 46(10): 1207-1216.
TrueMed-ForLivingMore
Κοινοποιήστε


Ιωάννης Κουκουλίθρας
Συντάκτης
O Ιωάννης Κουκουλίθρας είναι τριτοετής φοιτητής ιατρικής του Πανεπιστημίου Ιωαννίνων. Τα ενδιαφέροντά του επικεντρώνονται στη νευροφυσιολογία και αντιμετώπιση του χρόνιου πόνου, στις νευρολογικές παθήσεις , στις διαταραχές ύπνου και στις μυοσκελετικές παθήσεις. Έχει συμμετάσχει σε πολλά νευρολογικά και ορθοπεδικά συνέδρια. Είναι κάτοχος BLS, B-CON από το 2018 του Ευρωπαϊκού Συμβουλίου Αναζωογόνησης. Είναι μέλος της Αμερικανικής Ακαδημίας Νευρολογίας (American Academy of Neurology,AAN). Είναι βοηθός του εργαστηρίου Ανατομίας , Ιστολογίας, Εμβρυολογίας της Ιατρικής του Παν. Ιωαννίνων. Έχει μέχρι στιγμής (28/3/2020) 3 επιστημονικές δημοσιεύσεις.
Σπυρίδων Κολοκώτσιος
Συντάκτης
Ο Σπυρίδων Κολοκώτσιος είναι φοιτητής στο 4ο ακαδημαϊκό έτος του Πανεπιστημίου Δυτικής Αττικής του τμήματος Φυσικοθεραπείας.Τα ενδιαφέροντα του βασίζονται στην αντιμετώπιση του χρόνιου πόνου και στις μυοσκελετικές διαταραχές. Είναι πιστοποιημένος ως CKTP και έχει συμμετάσχει σε πληθώρα σεμιναρίων εκ των οποίων μερικά από αυτά είναι: Arthro tools Instrument Assisted Soft Tissue Mobilization,Kinesio Taping Assessments Fundamental Concepts and Techniques – International, Kinesio Taping Clinical Reasoning and Advanced Techniques, Mention Prevention
Αλεξάνδρα Σταμούλη
Συντάκτρια
Η Αλεξάνδρα Σταμούλη εισήχθη 8η στο Τμήμα Φυσικοθεραπείας του Πανεπιστημίου Δυτικής Αττικής και φοιτεί στο 4ο ακαδημαϊκό έτος. Στόχο της αποτελεί η ενασχόληση πάνω στην αντιμετώπιση μυοσκελετικών και νευρολογικών παθήσεων και η έρευνα για την ανάπτυξη και τεκμηρίωση καινούριων φυσικοθεραπευτικών μεθόδων και τεχνικών.
Μηνάς Πλεξουσάκης
Συντάκτης
Ο Μηνάς Πλεξουσάκης είναι φοιτητής στο 4ο ακαδημαϊκό έτος του Πανεπιστημίου Δυτικής Αττικής του τμήματος Φυσικοθεραπείας. Κυρίαρχο ενδιαφέρον του είναι τα μυοσκελετικά προβλήματα και αντιμετώπιση του χρόνιου πόνου. Παράλληλα ασχολείται και με νευρολογικά περιστατικά έχοντας ως βασικό στόχο την βελτίωση της λειτουργικότητας τους μέσω εκσυγχρονισμένων προγραμμάτων φυσικοθεραπείας.
ΔΙΑΒΑΣΤΕ ΕΠΙΣΗΣ
© 2019 TrueMed Media. All rights reserved. Our website services, content, and products are for informational purposes only. TrueMed Media does not provide medical advice, diagnosis, or treatment.