Τελικά το Parkinson περνάει… από το έντερο
![]() 30-3-2021
30-3-2021
![]() Αντιγόνη Βαρσάμη
Αντιγόνη Βαρσάμη

Λέξεις κλειδιά: νόσος Parkinson, νευροφλεγμονή, έντερο, α–συνουκλεΐνη (α-Syn), έγκλειστα παθολογικής α-Syn (σωμάτια Lewy), πνευμονογαστρικό νεύρο
Λίγο έως πολύ όλοι μας θα έχουμε ακούσει για τη νόσο του Parkinson (PD – Πάρκινσον) ή ακόμη θα έχουμε κάποιο άτομο στο περιβάλλον μας που πάσχει από αυτή. Πρόκειται για μια νευροεκφυλιστική ασθένεια του Κεντρικού Νευρικού Συστήματος (ΚΝΣ) με πλήθος φαινοτυπικών εκδηλώσεων στους ασθενείς, τόσο κινητικές όσο και μη-κινητικές. Τι σημαίνει, όμως, αυτό; Τα συμπτώματα της περιεγράφηκαν για πρώτη φορά πριν 200 χρόνια και, πιο συγκεκριμένα, το 1817 από τον James Parkinson στο κλασσικό μονόγραφό του “Essay on the Shaking Palsy”. Πολύ συνοπτικά, βασικά χαρακτηριστικά της νόσου αυτής είναι ο σχηματισμός των σωμάτιων Lewy, η μείωση στα επίπεδα ντοπαμίνης και ο εκφυλισμός των ντοπαμινεργικών νευρώνων σε διακριτές περιοχές του εγκεφάλου. Συνέπεια των γεγονότων αυτών, η διαταραχή των κινήσεων και όλο το φάσμα των συμπτωμάτων που παρουσιάζει ένας ασθενής. Με απλά λόγια, θα λέγαμε πως, με όλο και λιγότερα επίπεδα ντοπαμίνης, το άτομο έχει όλο και μικρότερη ικανότητα να ελέγξει τις κινήσεις, το σώμα και τα συναισθήματά του. Η αιτιοπαθογένεια της νόσου μέχρι και σήμερα είναι ασαφής, ωστόσο έχει συσχετισθεί με γεγονότα που επιδρούν στη διατάραξη της πρωτεϊνικής ομοιόστασης, της μιτοχονδριακής λειτουργίας, των επιπέδων ντοπαμίνης, της λειτουργίας ιόντων ασβεστίου, ενώ σε ορισμένες των περιπτώσεων φαίνεται να εμπλέκεται και ο γενετικός παράγοντας, αλλά και η νευροφλεγμονή.
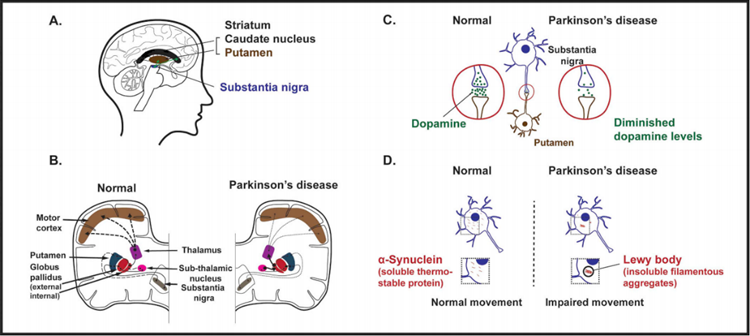
Σύγκριση φυσιολογικού & παθολογικού εγκεφάλου με νόσο Parkinson
«Συνήθως επηρεάζει τους ηλικιωμένους, σε παγκόσμια κλίμακα, το οποίο σημαίνει ότι παρατηρούνται υψηλότερα ποσοστά εμφάνισης της νόσου σε μεγαλύτερους ηλικιακά ανθρώπους. Απ’ ότι φαίνεται, ειδικότερα, εμφανίζεται περίπου στο 0.3% του γενικού πληθυσμού και σε ποσοστό 1-3% του πληθυσμού άνω των 65. Επιπλέον, η νόσος του Parkinson αποτελεί τη 4η συχνότερη νευρολογική ασθένεια σε άτομα άνω των 65 χρονών.»
Μέχρι εδώ, θα ήταν πολύ λογικό, να συμπεράνει κανείς πως πρόκειται για μία νόσο η οποία έχει τις απαρχές της εμφάνισής της και επηρεάζει πρωταρχικά δομές του εγκεφάλου. Και, εν μέρει τουλάχιστον, αυτό είναι αλήθεια. Ωστόσο, στην προσπάθεια ερευνητών αναζήτησης εδώ και μερικά χρόνια της αιτίας της νόσου και στο έντερο, αρκετά είναι τα νέα ερευνητικά δεδομένα που έχουν προκύψει, τα οποία ενισχύουν τη θεωρία πυροδότησης της νόσου του Parkinson, αρχικά από το έντερο και όχι από τον ίδιο τον εγκέφαλο! Και πολλοί θα αναρωτηθούν πως είναι αυτό δυνατό, όμως, αν το σκεφτεί κανείς λίγο καλύτερα και εξετάσει προσεκτικά όλα τα νεότερα δεδομένα, θα διαπιστώσει πως δεν είναι και τόσο παράλογη η θεωρία αυτή.
Καταρχάς, είναι γνωστό πως το έντερο αποτελεί μέρος του Νευρικού Συστήματος και πιο συγκεκριμένα, είναι τμήμα του Αυτόνομου Νευρικού Συστήματος του Απαγωγού σκέλους του Περιφερικού Νευρικού Συστήματος. Το τοίχωμα του γαστρεντερικού σωλήνα νευρώνεται από δύο δίκτυα αυτόνομων νευρώνων, αυτό του μυεντερικού και του υποβλεννογόνιου νευρικού πλέγματος (Εντερικό Νευρικό Σύστημα). Παρόλο που πολλά νευρικά αντανακλαστικά περιορίζονται εντός του γαστρεντερικού σωλήνα και άρα τον καθιστούν ανεξάρτητο του ΚΝΣ (Κεντρικό Νευρικό Σύστημα), πολλές είναι οι νευρικές ίνες του Συμπαθητικού και του Παρασυμπαθητικού Νευρικού Συστήματος που εισέρχονται στην εντερική οδό, καθιστώντας δυνατή την αλληλεπίδραση μεταξύ εντερικού πλέγματος και ΚΝΣ.
Αυτά, βέβαια, ήταν στοιχεία γνωστά εδώ και πάρα πολλά χρόνια, χωρίς όμως να προκύπτουν από αυτά άμεσες αποδείξεις για την απαρχή της νόσου Parkinson, παρά μόνο ενδείξεις για την υπόθεση συσχέτισης της νόσου με το έντερο -τουλάχιστον από το 2003. Το νέο στοιχείο, το οποίο είναι αυτό που ενισχύει περαιτέρω την προηγούμενη υπόθεση με νέες ενδείξεις, είναι η ένδειξη σχηματισμού της τοξικής πρωτεΐνης α-συνουκλεΐνης (α-Syn) στο έντερο, και η ύστερη μεταφορά της στον εγκέφαλο.
Η α-Syn είναι μια προσυναπτική νευρωνική πρωτεΐνη που συσχετίζεται γενετικά και νευροπαθολογικά με τη νόσο PD, Κωδικοποιείται από το γονίδιο SNCA, περιλαμβάνει 140 αμινοξικά κατάλοιπα και έχει βρεθεί ότι σε διαλυτή μορφή δεν λαμβάνει κάποια καθορισμένη δομή. Φυσιολογικά, σχηματίζει α-ελικοειδείς μορφές μέσα από τις οποίες προσδένεται σε αρνητικά φορτισμένα λιπίδια, πχ φωσφολιπίδια κυτταρικών μεμβρανών και δομές πλούσιες σε β-φύλλα σε περιόδους μακράς επώασης.

Πεπτίδιο α-Syn
H α-Syn εκφράζεται σε αφθονία στο νευρικό σύστημα, καθώς ξέρουμε πως αποτελεί το 1% της συνολικής κυτταροπλασματικής πρωτεΐνης. Η έκφραση της α-Syn, γενικά, επάγεται κατά τη νευρική ανάπτυξη. Επιπλέον, τα επίπεδα της επίσης υφίστανται ρύθμιση σε καταστάσεις που αλλάζουν την πλαστικότητα, ή στην περίπτωση κάποιου τραύματος, γεγονότα που οδηγούν στο συμπέρασμα ότι ίσως αποτελεί βασικό ρυθμιστή της συναπτικής διαβίβασης. Η συσσώρευση, λοιπόν, της παθολογικής μορφής της α-Syn, έχει ως αποτέλεσμα τη δημιουργία συσσωματωμάτων (εγκλείστων – σωμάτια Lewy), τα οποία οδηγούν στην παθογένεση της νόσου PD, αιτία για την οποία δεν υπάρχει θεραπεία παρά μόνο διαχείριση και επιβράδυνση των συμπτωμάτων. Τα συσσωματώματα αυτά δημιουργούνται λόγω της τάσης της α-Syn, να αναδιπλώνεται εσφαλμένα, και έτσι να γίνεται αδιάλυτη και να σχηματίζει πλούσια σε β- φύλλα αμυλοειδή συσσωματώματα που συσσωρεύονται και σχηματίζουν τα ενδοκυτταρικά αυτά έγκλειστα.
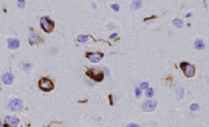
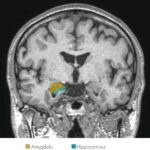
Παθολογικές συσσωρεύσεις (σωμάτια Lewy) α-Syn στην αμυγδαλή (Amyg)
Είναι γνωστό πως η μετάδοση της παθολογικής μορφής της αποτελεί μια από τις αιτιο-παθογένειες του Parkinson, καθώς και «σήμα κατατεθέν» στον εγκέφαλο των ασθενών με τη νόσο.
Γνωρίζοντας, λοιπόν, όλα αυτά, η υπόθεση πυροδότησης της νευροεκφυλιστικής αυτής νόσου από το έντερο, μοιάζει ολοένα και πιο λογική. Μένει τώρα, να γίνει κατανόηση των δεδομένων που οδήγησαν τους ερευνητές σ’ αυτή την υπόθεση.
Ειδικότερα, η ερευνητική ομάδα της Ιατρικής Σχολής του Πανεπιστημίου Johns Hopkins της Βαλτιμόρης, με επικεφαλής τον καθηγητή νευρολογίας Ted M. Dawson, δημοσίευσαν στο περιοδικό Neuron, την πειραματική μελέτη τους, με την οποία προσπάθησαν να ενισχύσουν τη θεωρία του Heiko Braak – Γερμανός ανατόμος που έχει ασχοληθεί εκτενώς με τη νόσο του Parkinson και την παθοφυσιολογία της – σχετικά με τη δυνατότητα διάδοσης της α-Syn από το έντερο στον ανθρώπινο εγκέφαλο μέσω του πνευμονογαστρικού νεύρου. Πιο συγκεκριμένα, χρησιμοποιώντας πειραματόζωα – ποντικούς, αξιολόγησαν τον βαθμό μετάδοσης της παθολογικής α-Syn στον εγκέφαλο των ποντικών – μοντέλων, μετά από την αρχική έγχυσή της στο δωδεκαδακτυλικό και πυλωρικό μυϊκό στρώμα των ποντικών.
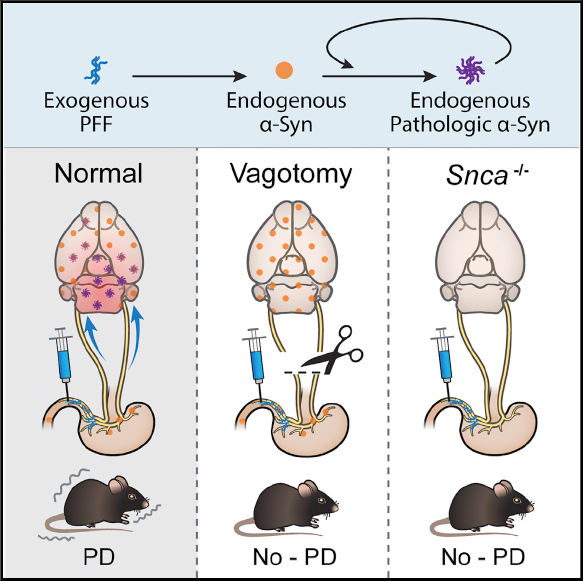
Περιληπτική απεικόνιση της ερευνητικής μελέτης
Η ομάδα παρατήρησε εξάπλωση της παθολογικής α-συν στον εγκέφαλο, όπως αξιολογείται από τη φωσφορυλίωση της Σερίνης 129 της πρωτεΐνης α-Syn, αρχικά, σε διάστημα ενός μήνα, στον πυρήνα του ραχιαίου κινητήρα, στη συνέχεια στα ουραία τμήματα του οπίσθιου εγκεφάλου, συμπεριλαμβανομένων των locus coeruleus, σχεδόν δύο μήνες μετά στην αμυγδαλή, στον ραχιαίο πυρήνα και στη φαιά ουσία pars compacta, ενώ πολύ αργότερα (επτά μήνες μετά), είχε πλέον διεισδύσει σε ζωτικές περιοχές, όπως ο ιππόκαμπος. Επιπλέον, απώλεια ντοπαμινεργικών νευρώνων, καθώς και κινητικά και μη κινητικά συμπτώματα (κατάθλιψη, απώλεια αίσθησης όσφρησης, προβλήματα μνήμης και μάθησης κ.ά.) παρατηρήθηκαν σε παρόμοιο χρονικό διάστημα. Επίσης, παρατηρήθηκε πως τα κολοβακτηρίδια της βαγοτομής – η διατομή των κλάδων του πνευμονογαστρικού νεύρου που έχει ως αποτέλεσμα τη μείωση έκκρισης γαστρικού οξέος – και ανεπάρκεια α-Syn, παρεμπόδισαν την εξάπλωση της α-συνουκλεοπάθειας από το έντερο στον εγκέφαλο, καθώς και τον σχετικό νευροεκφυλισμό και ελλείμματα συμπεριφοράς.
Κι ενώ όλα αυτά τα νέα ευρήματα ενισχύουν την ισχύ της θεωρίας του Braak, οι ερευνητές πιθανολογούν ότι τα ευρήματά τους ισχύουν και για τους ανθρώπους – κάτι που μένει να επιβεβαιωθεί –, απαραίτητη γνώση για τη θεραπευτική αντιμετώπιση της νόσου αποτελεί ο ακριβής τρόπο με τον οποίο γίνεται η εξάπλωση των σωματίων Lewy από το έντερο σε όλα αυτά τα σημεία του εγκεφάλου.
Υπάρχουν τρεις θεωρίες επ’ αυτού, με πρώτη την ήδη αναφερθείσα, την οδό του πνευμονογαστρικού νεύρου (vagus nerve), την απευθείας σύνδεση των εντερικών νεύρων με τον εγκέφαλο.
Η δεύτερη υπόθεση αφορά την επικοινωνία εντέρου και εγκεφάλου μέσω του ανοσοποιητικού συστήματος. Το αλληλόμορφο (N2081D) του γονιδίου LRRK2, με ρόλο στο ανοσοποιητικό σύστημα, είναι παράγοντας κινδύνου για τη νόσο του Crohn, η οποία προκαλεί φλεγμονή του βλεννογόνου του εντέρου. Επηρεάζει την ηλικία εμφάνισης της φλεγμονής, τη θέση στο έντερο την αυτοφαγία. Είναι πολύ ενδιαφέρον ότι αυτό το αλληλόμορφο είναι δείκτης κινδύνου και για τη νόσο του Parkinson. Η ανάλυση μιας μεγάλης βάσης δεδομένων όπου καταγράφονταν τα συμπτώματα και οι συνταγογραφήσεις των ασθενών, έδειξε ότι οι άνθρωποι με νόσο του Crohn είχαν 28% μεγαλύτερη πιθανότητα να εμφανίσουν Parkinson. Αλλά όσοι από αυτούς λάμβαναν στη θεραπεία τους τον αντιφλεγμονώδη παράγοντα αντι-TNFα (ανταγωνιστή του παράγοντα-α νέκρωσης των όγκων, TNF-α), είχαν 78% μικρότερο κίνδυνο εμφάνισης της νόσου.
Η τρίτη και τελευταία υπόθεση αφορά στα βακτήρια τα οποία φυσιολογικά υπάρχουν στο έντερο. Οι νευρώνες του στομάχου διαχωρίζονται από τα μικρόβια που κατοικούν εκεί, μόλις από μια στοιβάδα κυττάρων. Ο μικροβιολόγος Sarkis Mazmanian, στα πλαίσια μιας μελέτης που διεξήγαγε χρησιμοποιώντας ως πειραματόζωα ποντίκια, διαπίστωσε διαπίστωσε πως ασθενείς με Parkinson αντιμετωπίζουν γαστρεντερικές διαταραχές. Έτσι, μελέτησε τα βακτήρια του στομάχου σε γενετικά τροποποιημένα ποντίκια που υπερπαρήγαγαν α-Syn. Ουσιαστικά, αυτό που ήθελε να εξετάσει, ήταν αν η παρουσία ή η απουσία βακτηρίων επηρεάζει τα συμπτώματα. Μετά από τη σειρά αυτή πειραμάτων του, συμπέρανε πως απουσία βακτηρίων, τα συμπτώματα του Parkinson υποχωρούσαν. Παρόλο που συνέχιζαν να υπερπαράγουν α-Syn, δεν είχαν προβλήματα βάδισης ή ισορροπίας, ούτε δυσκοιλιότητα. Όταν μετέφερε τη μικροχλωρίδα ανθρώπων διαγνωσμένων με Parkinson σε ποντίκια που δεν είχαν μικροχλωρίδα, τα ποντίκια εμφάνισαν τα συμπτώματα της νόσου. Τα συμπτώματα μάλιστα ήταν λιγότερο έντονα στα ποντίκια που έλαβαν τη μικροχλωρίδα υγιών ανθρώπων.
Επίσης, έχει φανεί ότι οι άνθρωποι που έχουν αφαιρέσει τη σκωληκοειδή τους απόφυση έχουν μικρότερο κίνδυνο εμφάνισης της νόσου του Parkinson. Ο ρόλος της σκωληκοειδούς απόφυσης αρχίζει να αποσαφηνίζεται, καθώς φαίνεται ότι παίζει ρόλο στην υγεία του εντέρου. Συμβάλει στην άμυνα του οργανισμού, καθώς παράγει ανοσοσφαιρίνες και είναι σημαντική για την μικροβιακή ισορροπία του παχέος εντέρου, λειτουργώντας ως αποθήκη μικροβίων.
Τα πειράματα αυτά μας κάνουν να υποθέτουμε ότι κάτι στη μικροχλωρίδα του εντέρου πυροδοτεί τη λανθασμένη αναδίπλωση της α-Syn. Οι αποικίες βακτηρίων σχηματίζουν βιοµεµβράνες (biofilms), που συγκρατούνται από ένα πεπτίδιο που παράγουν τα ίδια, το αμυλοειδές. Τα αμυλοειδή δεν είναι βλαβερά για τον οργανισμό μας, καθώς χρησιμεύουν στην αποθήκευση πρωτεϊνών για μελλοντική χρήση. Επειδή όμως έχουν εντοπισθεί αμυλοειδείς μορφές της α-Syn σε σωμάτια Lewy, μας κάνει να πιστεύουμε ότι εμπλέκονται σε νευροεκφυλιστικές ασθένειες όπως το Parkinson.
Ίσως το πρόβλημα ξεκινά όταν συγκεντρώνονται στο λάθος σημείο.
Όταν τα βακτήρια «στρεσσάρονται», παράγουν πρωτεΐνες σε αμυλοειδή μορφή. Το σήμα που στέλνουν ίσως λαμβάνεται από τους γειτονικούς νευρώνες, στο στομάχι για να κάνουν το ίδιο. Η συγκέντρωση αμυλλοειδών στο στομάχι πυροδοτεί το σχηματισμό αμυλλοειδών στον εγκέφαλο. Μια προσέγγιση για την καθυστέρηση της ασθένειας, βασιζόμενη σ’ αυτή τη γνώση, είναι η ανάπτυξη αντισωμάτων που θα στοχεύουν την λανθασμένα αναδιπλωμένη α-Syn, από κύτταρο σε κύτταρο, μια θεραπευτική μέθοδος που είναι ήδη στα στάδια της ανάπτυξης σε μορφή φαρμάκου.
Τελικά, αναλογιζόμενοι όλα τα παραπάνω νεότερα ερευνητικά δεδομένα, θα λέγαμε πως πιθανώς ανοίγει ο δρόμος για να μπει τροχοπέδη στη νόσο σε διάφορα στάδια, ακόμη και προτού εμφανισθούν τα πρώτα συμπτώματα.
Πηγές
- Jiang, Chunmei et al. ‘The Gut Microbiota and Alzheimer’s Disease’. 1 Jan. 2017 : 1 – 15.
- Quigley EMM. Microbiota-Brain-Gut Axis and Neurodegenerative Diseases. Curr Neurol Neurosci Rep. 2017 Oct 17;17(12):94. doi: 10.1007/s11910-017-0802-6. PMID: 29039142.
- Szablewski, Leszek. ‘Human Gut Microbiota in Health and Alzheimer’s Disease’. 1 Jan. 2018 : 549 – 560.
- Leonidas Stefanis, a-Synuclein in Parkinson’s Disease, s Cold Spring Harb Perspect Med 2012;4:a009399
- Lippincott, Φαρμακολογία, 6η έκδοση, Επιστημονικές εκδόσεις Παρισιάνου Α.Ε., 2015, σελ 111-112
- Lavedan, Christian. “The synuclein family.” Genome research 8.9 (1998): 871-880.
- Transneuronal Propagation of Pathologic α-Synuclein from the Gut to the Brain Models Parkinson’s Disease, NeuronVol. 103Issue 4p627–641.e7Published online: June 26, 2019 Sangjune KimSeung-Hwan KwonTae-In KamNikhil PanickerSenthilkumar S. KaruppagounderSaebom Lee and others
- «Pathological a-Synuclein Transmission Initiates Parkinson-like Neurodegeneration in Nontransgenic Mice», Kelvin C. Luk et al., DOI: 10.1126/science.1227157, Science 338, 949 (2012);
- Braak, H., Del Tredici, K., Rüb, U., De Vos, R. A., Steur, E. N. J., & Braak, E. (2003). Staging of brain pathology related to sporadic Parkinson’s disease. Neurobiology of aging, 24(2), 197-211.
- Challis, C. (2016). Progression of Parkinson’s-like pathology following inoculation of alpha-synuclein preformed fibrils in the gut. Neuroscience.
- Hui, K. Y., Fernandez-Hernandez, H., Hu, J., Schaffner, A., Pankratz, N., Hsu, N. Y., … & Rivas, M. (2018). Functional variants in the LRRK2 gene confer shared effects on risk for Crohn’s disease and Parkinson’s disease. Science translational medicine, 10(423), eaai7795.
- Peter, I., Dubinsky, M., Bressman, S., Park, A., Lu, C., Chen, N., & Wang, A. (2018). Anti–tumor necrosis factor therapy and incidence of Parkinson disease among patients with inflammatory bowel disease. JAMA neurology.
- Sampson, T. R., Debelius, J. W., Thron, T., Janssen, S., Shastri, G. G., Ilhan, Z. E., … & Chesselet, M. F. (2016). Gut microbiota regulate motor deficits and neuroinflammation in a model of Parkinson’s disease. Cell, 167(6), 1469-1480.
- Friedland, R. P., & Chapman, M. R. (2017). The role of microbial amyloid in neurodegeneration. PLoS pathogens, 13(12), e1006654.
- Mao, X., Ou, M. T., Karuppagounder, S. S., Kam, T. I., Yin, X., Xiong, Y., … & Kang, H. C. (2016). Pathological α-synuclein transmission initiated by binding lymphocyte-activation gene 3. Science, 353(6307), aah3374.
Κοινοποιήστε



Αρχές Βιοηθικής και Διαχείρισης των Ζώων στην Βιοϊατρική Έρευνα και την Κτηνιατρική Επιστήμη
Η παρούσα μελέτη, προσεγγίζοντας το ζήτημα των καινοτόμων θεραπευτικών σχημάτων επιχειρεί να αναδείξει το ευρύτερο πλαίσιο και τις αρχές στο πεδίο της βιοηθικής και διαχείρισης των ζώων στην βιοϊατρική έρευνα και την κτηνιατρική επιστήμη

Βήμα προς βήμα το θερμικό σοκ σε ένα βρέφος
Το θερμικό σοκ σε βρέφη είναι ταχύτατα εξελισσόμενο και δυνητικά θανατηφόρο.
Κάθε λεπτό καθυστέρησης αυξάνει τον κίνδυνο βλάβης ή θανάτου.
ΡΟΗ ΕΙΔΗΣΕΩΝ
ΔΙΑΒΑΣΤΕ ΕΠΙΣΗΣ
Βρείτε μας στο Facebook και στο Instagram
Επικοινωνία
Η ομάδα μας
Διαφημιστείτε στη truemed.gr
Όροι χρήσης
Προσωπικά δεδομένα
Copyright©Truemed
Για περισσότερη ζωή
Designed – Developed by Premiumweb.gr
| Επικοινωνία | Η ομάδα μας | Διαφημιστείτε στη truemed.gr| | Όροι χρήσης | Προσωπικά δεδομένα | Copyright©Truemed | |Για περισσότερη ζωή |
Designed – Developed by Premiumweb.gr

© 2019 TrueMed Media. All rights reserved. Our website services, content, and products are for informational purposes only. TrueMed Media does not provide medical advice, diagnosis, or treatment.
Αρθρογράφος
Η Αντιγόνη Βαρσάμη γεννήθηκε το 1998 στην Αθήνα, ενώ κατάγεται από τον Τύρναβο Λάρισας, όπου και μεγάλωσε. Είναι τεταρτοετής φοιτήτρια του τμήματος Μοριακής Βιολογίας & Γενετικής στην Αλεξανδρούπολη, κι εκπονεί την πτυχιακή της εργασία στο Εργαστήριο Γενετικής του τμήματος Ιατρικής του Δημοκριτείου Πανεπιστημίου Θράκης. Έχει γνώσεις αγγλικών επιπέδου C2 και γαλλικών επιπέδου B2. Η αγάπη της για τη γραφή, σε συνδυασμό με το ατέρμονο ενδιαφέρον της για την επιστήμη, την ώθησαν να ξεκινήσει, τον Νοέμβριο του 2019, τη συγγραφή άρθρων στην TrueMed προσεγγίζοντας διάφορα θέματα βιολογικού περιεχομένου, πράγμα που συνεχίζει μέχρι σήμερα και ελπίζει να μπορεί να εξακολουθεί και στο μέλλον. Μελλοντικό της στόχο αποτελεί η περεταίρω εξειδίκευση και ενασχόληση με τον τομέα της Κυτταρογενετικής, Ιατρικής Γενετικής και Εξωσωματικής γονιμοποίησης.
Λοιπά προσόντα
ΞΕΝΕΣ ΓΛΩΣΣΕΣ
Αγγλικά: Κάτοχος του Michigan State University English Language Examination MSU-CELP (C2)
Γαλλικά: Κάτοχος του DELFB2 και του Κρατικού Πιστοποιητικού Γλωσσομάθειας ΚΠγ Β2
ΟΡΓΑΝΩΤΙΚΕΣ ΚΑΙ ΚΟΙΝΩΝΙΚΕΣ ΔΕΞΙΟΤΗΤΕΣ ΚΑΙ ΙΚΑΝΟΤΗΤΕΣ
Μπορεί να εργαστεί υπό συνθήκες μεγάλης πίεσης και έχοντας τη δυνατότητα να ανταπεξέλθει και να αποδώσει σε αυτές, ενώ είναι δεκτική στην ομαδική συνεργασία για ένα καλό αποτέλεσμα σε κάθε τομέα. Η οργάνωση, η επιμονή στη λεπτομέρεια και η συνέπεια αποτελούν στοιχεία που την χαρακτηρίζουν.
ΤΕΧΝΙΚΕΣ ΚΑΙ ΚΑΛΛΙΤΕΧΝΙΚΕΣ ΔΕΞΙΟΤΗΤΕΣ ΚΑΙ ΙΚΑΝΟΤΗΤΕΣ
Κάτοχος Πιστοποίησης Επάρκειας Εκτελωνιστή (72/2019) (Βόλος, Οκτώβριος 2019)
Γνώση Η/Υ, Windows, Excel, Power Point, Internet
Κάτοχος άδειας οδήγησης αυτοκινήτου
Πιάνο
Στον ελεύθερο χρόνο της, διαβάζει βιβλία, περνάει χρόνο με αγαπημένα της πρόσωπα, ενώ απολαμβάνει τις μεγάλες βόλτες στη θάλασσα και την εξοχή.
Αγαπημένη εποχή:Καλοκαίρι
Αγαπημένο χρώμα:Μπλε
Μεγαλύτερος φόβος:Να χάσει τους αγαπημένους της ανθρώπους
Αγαπημένο είδος βιβλίων:Ιστορικά μυθιστορήματα
Αγαπημένοquote:«Υπάρχει μόνο ένα πράγμα που κάνει ένα όνειρο να επιτευχθεί: ο φόβος της αποτυχίας» -PauloCoello
Emailεπικοινωνίας:antivarsami@gmail.com
Αριθμός άρθρων που έχει γράψει στην Truemed: 9